题目内容
7.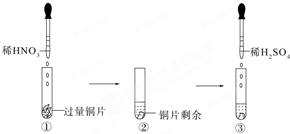 某实验过程如图所示:下列有关图③中出现的现象及解释合理的是( )
某实验过程如图所示:下列有关图③中出现的现象及解释合理的是( )| A. | 铜片溶解,因铜与稀H2SO4反应生成SO2 | |
| B. | 铜片溶解,产生无色气体,该气体为H2 | |
| C. | 无明显现象,因稀H2SO4不与铜反应 | |
| D. | 铜片溶解,产生无色气体,该气体在试管口变为红棕色 |
分析 由图可知,①中发生Cu与硝酸反应生成硝酸铜、NO和水,Cu过量,③中加硫酸,硝酸铜提供硝酸根离子、硫酸提供氢离子,与Cu发生氧化还原反应,以此来解答.
解答 解:③中加硫酸,硝酸铜提供硝酸根离子、硫酸提供氢离子,与Cu发生氧化还原反应,反应为3Cu+8H++2NO3-=Cu2++2NO↑+4H2O,可观察到铜片溶解,产生无色气体,该气体在试管口变为红棕色(NO被氧化为二氧化氮),
故选D.
点评 本题考查硝酸的性质及实验装置综合应用,为高频考点,把握发生的氧化还原反应及离子反应为解答的关键,侧重分析与应用能力的考查,注意硝酸盐的性质,题目难度不大

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
18.要加快H2O2分解的速度,下列措施不可行的是( )
| A. | 加热或光照 | B. | 加MnO2或FeCl3 | C. | 加压 | D. | 增大H2O2的浓度 |
15. 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
 元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )
元素周期表的形式多种多样,如图是扇形元素周期表的一部分(1~36号元素),对比中学常见元素周期表思考扇形元素周期表的填充规律,下列说法正确的是( )| A. | ④的最高价氧化物对应的水化物能与其氢化物反应,生成离子化合物 | |
| B. | ⑤的三种核素的化学性质不相同 | |
| C. | ⑥、⑧、⑨对应单核离子的半径依次增大 | |
| D. | ⑧、⑨两种元素的气态氢化物及其最高价氧化物的水化物均为强酸 |
2.对于在一密闭容器中进行如下反应:C(S)+O2(g)=CO2(g)下列说法错误的( )
| A. | 将木炭粉碎成粉末状可以加快化学反应速率 | |
| B. | 升高温度可以加快化学反应速率 | |
| C. | 增加压强可以加快化学反应速率 | |
| D. | 增加木炭的量可以加快化学反应速 |
12.下列变化属于化学变化的是( )
| A. | 碘的升华 | B. | 碘化银用于人工降雨 | ||
| C. | 液溴的气化 | D. | 漂白粉久置失效 |
19.下列关于化学反应中的能量变化的表述正确的是( )
| A. | 加热才能发生的反应一定是吸热反应 | |
| B. | 断开化学键的过程会吸收能量 | |
| C. | 化学能不仅可以与热能相互转化,还可以与电能相互转化 | |
| D. | 燃烧可能为吸热反应 |
16.可以证明某化合物一定含有离子键的性质是( )
| A. | 熔融状态能导电 | B. | 具有较高的熔点 | C. | 可溶于水 | D. | 溶于水能导电 |
 与NaOH的醇溶液共热制备CH3-CH═CH2
与NaOH的醇溶液共热制备CH3-CH═CH2 与适量NaHCO3溶液反应制备
与适量NaHCO3溶液反应制备