题目内容
短周期元素X、Y、Z在元素周期表中的位置如图,关于X、Y、 Z的说法正确的是 ( )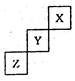
| A.相同条件下,三种元素的单质跟氢气反应时,X单质最剧烈 |
| B.由氢、氧和Z元素形成的常见化合物中既含有离子键又含有共价键 |
| C.ZO2能与Z的最高价氧化物对应的水化物反应生成Z单质 |
| D.Y的气态氢化物稳定性比Z的气态氢化物的稳定性强 |
D
解析试题分析:根据短周期元素X、Y、Z在元素周期表中的位置可知X、Y、 Z分别是He、F、S,则相同条件下,三种元素的单质跟氢气反应时,Y单质最剧烈,A不正确;B、由氢、氧和硫元素形成的常见化合物是硫酸,只有共价键,B不正确;C、SO2与硫酸不反应,C不正确;D、非金属性是氟强于硫,非金属性越强,氢化物的稳定性越强,则Y的气态氢化物稳定性比Z的气态氢化物的稳定性强,D正确,答案选D。
考点:考查元素周期表的结构和元素周期律的应用

练习册系列答案
 灵星计算小达人系列答案
灵星计算小达人系列答案
相关题目
下列物质的性质比较,正确的是
| A.酸性:H2SO4>HClO4>HBrO4 | B.碱性:NaOH>KOH>RbOH |
| C.非金属性: P>S>Cl | D.气态氢化物稳定性:HF>H2O>PH3 |
X和Y两种元素的核电荷数之和为22,X的原子核外电子数比Y的少6个。下列说法中不正确的是( )
| A.X的单质固态时为分子晶体 | B.Y的单质可以形成原子晶体 |
| C.X与Y形成的化合物固态时为分子晶体 | D.X与碳形成的化合物为分子晶体 |
关于原子结构、元素性质的说法正确的是
| A.随原子序数的递增,元素原子的核外电子数增多,原子半径逐渐减小 |
| B.若两种不同的核素具有相同的中子数,则二者一定不属于同种元素 |
| C.在化学反应中,原子首先失去的电子能量最低 |
| D.在元素周期表中,各主族元素的最高化合价与其族序数相等 |
下列叙述正确的是( )
| A.碱金属单质在空气中燃烧的生成物都是过氧化物 |
| B.少量的碱金属单质都能保存在煤油中 |
| C.HF、HCl、HBr、HI的稳定性、还原性从左到右依次减弱 |
| D.随着原子序数的递增,卤素单质的颜色由浅到深,熔沸点逐渐升高 |
科学家根据元素周期律和原子结构理论预测,原子序数为114的元素属于第七周期ⅣA族, 称为类铅元素。下面关于它的原子结构和性质预测正确的是
| A.类铅元素原子的最外层电子数为4 | B.其常见价态为+2、+3、+4 |
| C.它的金属性比铅弱 | D.它的原子半径比铅小? |
据报道,N4是一种形似白磷的分子,18O2是比黄金还贵重的物质。下列说法正确的是
| A.18O2与16O2性质完全相同 | B.N4=2N2是化学变化 |
| C.N4和N2互为同位素 | D.18O2中含18个中子 |
运用元素周期律分析下面推断,其中错误的是( )
| A.铍(Be)的氧化物的水化物可能具有两性 |
| B.砹(At)为有色固体,HAt不稳定,AgAt感光性很强,但不溶于水也不溶于酸 |
| C.硫酸锶(SrSO4)是难溶于水的白色固体 |
| D.硒化氢(H2Se)是有色、有毒的气体,比H2S稳定 |