题目内容
9.可逆反应4NH3(g)+5O2 (g)?4NO(g)+6H2O(g),下列叙述能说明反应已达平衡状态的是( )| A. | 达到化学平衡时,υ正(NH3)=υ逆(H2O) | |
| B. | 达到化学平衡时,4υ (O2)=5υ (NO) | |
| C. | 若单位时间内生成x mol NO的同时,也消耗x mol NH3 | |
| D. | 若单位时间内生成4 mol NO的同时,也生成4 mol NH3 |
分析 根据化学平衡状态的特征解答,当反应达到平衡状态时,正逆反应速率相等,各物质的浓度、百分含量不变,以及由此衍生的一些量也不发生变化,解题时要注意,选择判断的物理量,随着反应的进行发生变化,当该物理量由变化到定值时,说明可逆反应到达平衡状态.
解答 解:A、正逆反应速率之比等于化学计量数之比时,反应才达到平衡状态,所以3υ正(NH3)=2υ逆(H2O)时,反应达到平衡状态,故A错误;
B、没有说明是正反应速率还是逆反应速率,且不符合速率之比等于化学计量数之比,故B错误;
C、生成 NO和消耗NH3,都是正反应,不能说明正逆反应速率相等,故C错误;
D、生成 NO和生成NH3的速率之比等于1:1,说明正逆反应速率相等,反应达到平衡状态,故D正确;
故选D.
点评 本题考查了化学平衡状态的判断,难度不大,注意当反应达到平衡状态时,正逆反应速率相等,但不为0.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
19.形成物质世界多样性的原因有:①元素种类 ②同位素 ③化学键成键方式 ④同分异构体现象 ⑤同素异形体现象( )
| A. | ①②③ | B. | ②④⑤ | C. | 仅①③ | D. | ①②③④⑤ |
4.下列说法正确的是( )
| A. | 原子最外层只有两个电子的元素都在第ⅡA族 | |
| B. | 人们通常在过渡元素中寻找催化剂和耐高温、耐腐蚀的合金材料 | |
| C. | 共价化合物中可能含有离子键 | |
| D. | 水溶液能导电的化合物都是离子化合物 |
18.下列各项表述正确的是( )
| A. | 羟基的电子式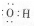 | B. | 醛基官能团符号-COH | ||
| C. | 乙醇的分子式:CH3CH2OH | D. | 异丁烷的结构简式:CH3CH(CH3)CH3 |
13.下列四个图象所反映的内容与相应反应符合的是(a、b、c、d均大于0)( )
| A. | 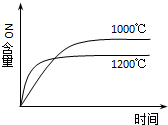 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-a kJ•mol-1 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-a kJ•mol-1 | |
| B. | 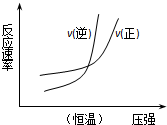 N2(g)+3H2(g)?2NH3(g)△H=-b kJ•mol-1 N2(g)+3H2(g)?2NH3(g)△H=-b kJ•mol-1 | |
| C. | 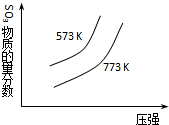 2SO3(g)?2SO2(g)+O2(g)△H=+c kJ•mol-1 2SO3(g)?2SO2(g)+O2(g)△H=+c kJ•mol-1 | |
| D. | 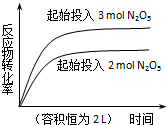 2N2O5(g)?4NO2(g)+O2(g)△H=+d kJ•mol-1 2N2O5(g)?4NO2(g)+O2(g)△H=+d kJ•mol-1 |
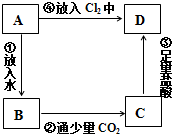
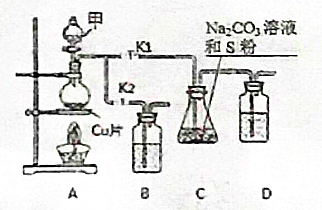 硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1.
硫代硫酸钠(Na2S2O3)在工业生产、医药制造业中被广泛应用,工业普遍使用Na2SO3与硫磺(S)共煮得到,装置如图1.