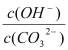题目内容
【题目】下列说法中正确的是
A. 在多电子的原子里,能量高的电子通常在离核较近的区域内运动
B. 凡单原子形成的稳定离子,一定具有稀有气体元素原子的8电子稳定结构
C. Na2O2属于离子化合物,熔化时只破坏离子键,不破坏O-O共价键
D. 俄国化学家道尔顿为元素周期表的建立作出了巨大贡献
【答案】C
【解析】A.在多电子的原子里,能量高的电子通常在离核较远的区域内运动,故A错误;B.单原子形成的稳定离子,不一定具有稀有气体元素原子的8电子稳定结构,如Fe3+,故B错误;C.Na2O2属于离子化合物,熔化时电离产生Na+、![]() ,只破坏离子键,不破坏O-O共价键,故C正确;D.俄国化学家门捷列夫为元素周期表的建立作出了巨大贡献,故D错误。故选C。
,只破坏离子键,不破坏O-O共价键,故C正确;D.俄国化学家门捷列夫为元素周期表的建立作出了巨大贡献,故D错误。故选C。

练习册系列答案
相关题目