题目内容
【题目】将两种不同物质的量浓度的Na2CO3溶液升高温度溶液中c(CO32-)变化如图所示,下列微粒的物质的量浓度关系正确的是( )
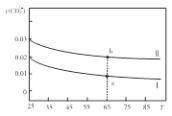
A.将溶液I升高温度,溶液pH减小
B.溶液a比溶液b中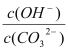 更大
更大
C.65℃时,向溶液a中加入1.06gNa2CO3固体,溶解后即为溶液b
D.溶液II一定存在:c(Na+)=2c(CO32-)+c(HCO3-)+c(OH-)
【答案】B
【解析】
试题分析:A.Na2CO3溶液升高温度时CO32-水解程度增大,溶液碱性增强,溶液pH增大,A错误;B.相同温度时,Na2CO3溶液浓度越小,CO32-水解程度越大,B正确;C.因题目中未指明溶液体积是1L,故不能确定溶液的浓度是多少,C错误;D.根据溶液中电荷守恒的规律,c(Na+)+c(H+)= 2c(CO32-)+c(HCO3-) + c(OH-),D错误。答案选B。

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
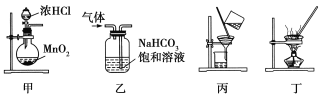
【题目】已知实验室制备1,2﹣二溴乙烷可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.现在用溴的CCl4溶液和足量的乙醇制备1,2﹣二溴乙烷的装置如下图所示:

有关数据列表如下:
乙醇 | 1,2﹣二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度/gcm﹣3 | 0.79 | 2.2 | 0.71 |
沸点/℃ | 78.5 | 132 | 34.6 |
熔点/℃ | 一l30 | 9 | ﹣1l6 |
回答下列问题:
(1)制备1,2﹣二溴乙烷的合成路线
(2)在装置C中应加入 ,(填正确选项前的字母)其目的是
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(3)装置B的作用是 ;
(4)若产物中有少量副产物乙醚.可用 的方法除去;
(5)反应过程中应用冷水冷却装置D,其主要目的是 ;但又不能过度冷却(如用冰水),其原因是 .