题目内容
下列关于化学反应与能量的说法正确的是( )
| A.化学反应中一定有物质变化但不一定有能量变化 |
B.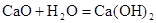 是放热反应,说明CaO的能量大于 是放热反应,说明CaO的能量大于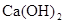 的能量 的能量 |
C.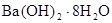 晶体与氯化铵晶体反应不需要加热就能发生,说明该反应是放热反应 晶体与氯化铵晶体反应不需要加热就能发生,说明该反应是放热反应 |
| D.由H2→2H的过程需要吸收能量 |
D
解析试题分析:A选项,在化学反应中一定有物质变化,并伴随着能连变化。化学反应中有旧键断裂、新化学键形成,所以一定有能量变化。B选项,反应物总能量大于生成物总能量,化学反应放出能量,反应放热。题目中缺少了水的能量。C选项 ,放热反应与反应过程是否须要加热无关。D选项正确,由氢分子别打破成为H原子,需破坏原有化学键,故需要加入能量,为吸热反应。
考点:考查化学反应能量变化规律。

已知:C(s,石墨) ="=" C(s,金刚石) ΔH =" +1.9" kJ·mol-1。下列有关说法正确的是
| A.相同条件下,1 mol石墨比1 mol金刚石能量高 |
| B.断裂1mol石墨中的化学键吸收的能量比断裂1mol金刚石中的化学键吸收的能量少 |
| C.若:C(s,石墨) + O2(g)==CO2(g) ΔH1=-393.5 kJ?mol-1 则有:C(s,金刚石) + O2(g)==CO2(g)ΔH2=-395.4 kJ·mol-1 |
| D.其他条件不变时,加入合适的催化剂,可实现该反应的反应热转变为ΔH<0 |
下列反应属于吸热反应的是
| A.碳与水蒸气制水煤气的反应 | B.生石灰和水的反应 |
| C.盐酸与氢氧化钠溶液的反应 | D.木炭在氧气中燃烧 |
下列说法或表示方法正确的是
| A.等物质的量的硫蒸气和固体硫分别完全燃烧,后者放出热量多 |
| B.由C(石墨)= C(金刚石) △H=+1.90 kJ/mol可知,金刚石比石墨稳定 |
| C.在101kPa时,2g氢气完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为: 2H2(g)+O2(g)=2H2O(l) △H=-285.8kJ/mol |
| D.在稀溶液中,H+(aq)+ OH-(aq)=H2O(l) △H=-57.3kJ/mol,若将含0.5molH2SO4的浓硫酸与含1molNaOH的溶液混合,放出的热大于57.3kJ |
已知反应:
①101 kPa时,2C(s)+O2(g) =2CO(g) ΔH=-221 kJ·mol-1
②稀溶液中,H+(aq)+OH-(aq) =H2O(l) ΔH=-57.3 kJ·mol-1
③在同温同压下,S(g)+O2(g)=SO2(g) ΔH1
下列结论正确的是( )
| A.H2SO4和Ba(OH)2反应的中和热ΔH=2×(-57.3)kJ/mol |
| B.C的标准燃烧热为-110.5 kJ·mol-1 |
| C.稀醋酸与稀NaOH溶液反应生成1 mol水放出的热量为57.3 kJ |
| D.由③知S(s)+O2(g)=SO2(g)ΔH2则ΔH2>ΔH1 |
已知下列四个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(g) △H1; 2H2S(g)+3O2(g)=2SO2(g)+2H2O(l) △H2;
2H2S(g)+O2(g)=2S(s)+2H2O(g) △H3; 2H2S(g)+O2(g)=2S(s)+2H2O(l) △H4;
则△H四者的关系中正确的是
| A.△H1>△H2>△H3>△H4 | B.△H4>△H2>△H3>△H1 |
| C.△H3>△H4>△H1>△H2 | D.△H4>△H3>△H2>△H1 |
已知:
| A.-393.5kJ/mol | B.-679.3 kJ/mol | C.-787 k J/mol | D.+180.9 kJ/mol |
下列说法正确的是( )
| A.反应热就是反应中放出的能量 |
| B.在101 kPa时,1 mol碳燃烧所放出的热量为碳的燃烧热 |
| C.等量的硫蒸气和硫固体分别完全燃烧,前者放出的热量多 |
| D.由C(石墨)→C(金刚石) ΔH=+1.9 kJ·mol-1可知,金刚石比石墨稳定 |
灰锡(以粉末状态存在)和白锡是锡的两种同素异形体。已知:
① Sn(s、白) + 2HCl(aq) → SnCl2(aq) + H2(g) + Q1
② Sn(s、灰) + 2HCl(aq) → SnCl2(aq) + H2(g) + Q2
 ③ Sn(s、灰)
③ Sn(s、灰)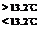 Sn(s、白) + Q3, Q3=" -" 2.1kJ
Sn(s、白) + Q3, Q3=" -" 2.1kJ
根据以上信息推断正确的是
| A.灰锡、白锡的互相转化是可逆反应 | B.常温下锡以灰锡状态存在 |
| C.反应中的能量变化:Q1 < Q2 | D.长期处于13.2℃以下,锡制器皿会自行毁坏 |