题目内容
3.碳元素在自然界中分布很广,在地壳中其丰富程度位列第14位,远低于氧、硅、铝、铁等元素.但是,碳却是存在形式最复杂的元素,如煤、石油、天然气、动植物体、石灰石、白云石、二氧化碳等.请回答下列问题:
(1)基态碳原子的电子排布式为1s22s22p2.
(2)在CO2分子中,碳原子采用sp杂化轨道与氧原子成键.
(3)COCl2俗称光气,分子中C原子采取sp2杂化成键,应用价层电子对互斥理论,预测COCl2分子的空间构型为平面三角形.
(4)二茂铁(C5H5)2Fe是Fe2+与环戊二烯基形成的一类配合物,实验室测定铁的含量:可用配位剂邻二氮菲(
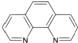 ),它能与Fe2+形成红色配合物(如图1),该配离子中Fe2+与氮原子形成配位键共有6个.
),它能与Fe2+形成红色配合物(如图1),该配离子中Fe2+与氮原子形成配位键共有6个.(5)普鲁士蓝可用作染料,它的结构如图2所示.普鲁士蓝中,n(K+):n(Fe3+):n(Fe2+):n(CN-)=1:1:1:6.
(6)CaC2晶体的晶胞结构与NaCl晶体相似,但CaC2晶体中哑铃C22-的存在,使晶胞沿一个方向拉长(如图3).CaC2中C22-与O22+互为等电子体,O22+的电子式可表示为
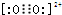 .已知CaC2晶体密度为ag•cm-3,NA表示阿伏加德罗常数,则CaC2晶胞体积为$\frac{256}{a{N}_{A}}$cm3.
.已知CaC2晶体密度为ag•cm-3,NA表示阿伏加德罗常数,则CaC2晶胞体积为$\frac{256}{a{N}_{A}}$cm3.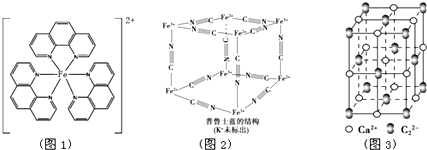
分析 (1)基态C原子核外有6个电子,根据构造原理书写其基态原子核外电子排布式;
(2)根据价层电子对互斥理论确定C原子杂化方式;
(3)C原子价层电子对个数是3且不含孤电子对,据此判断其空间构型;
(4)根据图1分析,Fe与N原子之间的键为配位键;
(5)利用均摊法计算以及电荷守恒来分析;
(6)等电子体结构和性质相似,根据C22-的结构书写O22+的电子式;利用均摊法计算出晶胞中含有CaC2的数目,再根据V=$\frac{m}{ρ}$计算.
解答 解:(1)基态C原子核外有6个电子,根据构造原理知C元素基态原子核外电子排布式为1s22s22p2,
故答案为:1s22s22p2;
(2)二氧化碳分子中C原子价层电子对个数是2且不含孤电子对,所以C原子采用sp杂化,故答案为:sp;
(3)C原子价层电子对个数是3且不含孤电子对,所以其空间构型为平面三角形,故答案为:平面三角形;
(4)Fe与N原子之间的键为配位键,由图1可知,该配离子中Fe2+与氮原子形成配位键共有6个,故答案为:6;
(5)Fe3+离子的个数为:4×$\frac{1}{8}$=$\frac{1}{2}$;Fe2+离子的个数为:4×$\frac{1}{8}$=$\frac{1}{2}$;CN一离子的个数为:12×$\frac{1}{4}$=3,
根据电荷守恒:N(K+)+N(Fe3+)×3+N(Fe2+)×2=N(CN一),得N(K+)=$\frac{1}{2}$,
普鲁士蓝中 n(K+):n(Fe3+):n(Fe2+):n(CN一)=1:1:1:6,
故答案为:1:1:1:6;
(6)等电子体结构和性质相似,根据C22-的结构知O22+的电子式为 ;CaC2晶胞含有Ca2+数目为12×$\frac{1}{4}$+1=4,含有C22-的数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则每个晶胞的质量为$\frac{4×64}{{N}_{A}}$g,晶胞的体积为V=$\frac{m}{ρ}$=$\frac{\frac{256}{{N}_{A}}}{{a}^{3}}$=$\frac{256}{a{N}_{A}}$cm3;
;CaC2晶胞含有Ca2+数目为12×$\frac{1}{4}$+1=4,含有C22-的数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则每个晶胞的质量为$\frac{4×64}{{N}_{A}}$g,晶胞的体积为V=$\frac{m}{ρ}$=$\frac{\frac{256}{{N}_{A}}}{{a}^{3}}$=$\frac{256}{a{N}_{A}}$cm3;
故答案为: ;$\frac{256}{a{N}_{A}}$.
;$\frac{256}{a{N}_{A}}$.
点评 本题考查物质结构和性质,涉及晶胞计算、核外电子排布式的书写、微粒空间构型判断、等电子体等知识点,根据等电子体特点、晶胞、价层电子对互斥理论等知识点分析解答即可,题目难度中等.

| A. | 氯化钠的晶体模型: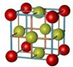 | |
| B. | 铍原子最外层的电子云图: | |
| C. | 次氯酸的结构式:H-O-Cl | |
| D. | CH3CHOHCH(CH3)2名称:2-3-二甲基丙醇 |
| A. | 常温下,10L pH=1的硫酸溶液中含有的H+数为NA | |
| B. | 将58.5g NaCl溶于1.00L水中,所得NaCl溶液的浓度为1.00mol•L-1 | |
| C. | 1molCl2与足量的铁反应,转移的电子数为3NA | |
| D. | 1molAl3+含有的核外电子数为3NA |
| A. | 28g N2、N2O、N2O4的混合气体含有氮原子数为2NA | |
| B. | 质量均为7.8 g Na2S、Na2O2的固体中含有的阴离子数均为0.1NA | |
| C. | 0.5 mol•L-1的乙酸溶液中,乙酸分子的数目小于0.5NA | |
| D. | 78g苯分子中含有碳碳双键数为3 NA |
| A. | D氢化物的稳定性比B氢化物的稳定性强 | |
| B. | 5种元素中,E元素氧化物的水合物的酸性最强 | |
| C. | A与B、D分别可形成AB2、AD2的化合物 | |
| D. | B和C可形成离子化合物,且C离子的半径大于B离子的半径 |