题目内容
20.如图实验操作或装置(略去部分夹持仪器)正确的是( )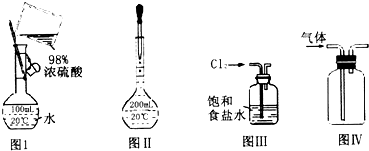
| A. | 图I表示为配制一定物质的量浓度稀硫酸时的操作 | |
| B. | 图Ⅱ表示为配制一定物质的量浓度的溶液定容时的操作 | |
| C. | 用图III所示装置吸收氯气中的氯化氢气体 | |
| D. | 用图IV所示装置收集一氧化氮气体 |
分析 A.容量瓶只能配制一定物质的量浓度溶液,不能稀释或溶解药品;
B.定容时,胶头滴管不能伸入容量瓶中;
C.洗气装置中导气管遵循“长进短出”原则,氯气不易溶于饱和食盐水中,HCl极易溶于水中;
D.NO易和氧气反应生成二氧化氮,且NO不溶于水,所以不能采用排空气集气法收集NO.
解答 解:A.容量瓶只能配制一定物质的量浓度溶液,不能稀释或溶解药品,应该先在烧杯中稀释浓硫酸,冷却至室温后再在容量瓶中配制一定物质的量浓度稀硫酸,故A错误;
B.定容时,胶头滴管不能伸入容量瓶中,否则易污染药品,故B错误;
C.洗气装置中导气管遵循“长进短出”原则,氯气不易溶于饱和食盐水中,HCl极易溶于水中,所以该装置能除去氯气中的氯化氢,故C正确;
D.NO易和氧气反应生成二氧化氮,且NO不溶于水,所以不能采用排空气集气法收集NO,应该采用排水集气法收集,故D错误;
故选C.
点评 本题考查化学实验方案评价,为高频考点,涉及气体收集、除杂、溶液配制等知识点,明确物质性质、实验基本操作方法即可解答,知道气体密度、溶解性与收集方法的关系,易错选项是B.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
10.已知氧化性Fe3+>I2.FeI2溶液中通入一定量的Cl2,发生反应的离子方程式为:a Fe2++bI-+c Cl2→d Fe3++e I2+f Cl-下列选项中的数字与离子方程式中的a、b、c、d、e、f一一对应,其中不符合反应实际的是( )
| A. | 2 0 1 2 0 2 | B. | 0 2 1 0 1 2 | ||
| C. | 2 4 3 2 2 6 | D. | 2 10 6 2 5 12 |
11.已知Co2O3在酸性溶液中易被还原成Co2+;则Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A. | Cl2+2FeCl2═2FeCl3 | B. | 3I2+6FeCl2═4FeCl3+2FeI3 | ||
| C. | Co2O3+6HCl═2CoCl2+Cl2↑+3H2O | D. | 2Fe3++2I-═2Fe2++I2 |
8.为了使稀硫化钠溶液中$\frac{c(N{a}^{+})}{c({S}^{2-})}$的比值变小,可加入的物质是( )
| A. | 适量的盐酸 | B. | 适量的NaOH溶液 | C. | 适量的FeCl2溶液 | D. | 适量的Na2S固体 |
15.下列有关物质的性质与应用正确且相对应的是( )
| A. | Na、K合金熔点低、沸点高,可用作原子反应堆导热液 | |
| B. | SiO2具有高沸点,可用作制备光导纤维 | |
| C. | NH3具有还原性,可用作制冷剂 | |
| D. | HF是强酸,可用于雕刻玻璃 |
12.下列说法正确的是( )
| A. | 根据反应2C+SiO2$\frac{\underline{\;高温\;}}{\;}$Si+2CO↑说明碳的非金属性强于硅的非金属性 | |
| B. | 加热分解CuSO4•5H2O过程中使用的玻璃仪器有酒精灯、坩埚、玻璃棒 | |
| C. | 最高化合价为+7的元素一定属于主族元素 | |
| D. | 16gO3含有8NA个电子 |
9.aL某浓度的SnC12溶液与过量FeC13溶液充分混合后,再加入$\frac{a}{2}$L 0.2000mol•L-1 K2Cr2O7溶液,恰好完全反应,则SnC12的浓度为(提示:①2Fe3++Sn2+═2Fe2++Sn4+;②6Fe2++Cr2O${\;}_{7}^{2-}$+14H+═6Fe3++2Cr3++7H2O)( )
| A. | 0.3000mol•L-1 | B. | 1.2000 mol•L-1 | C. | 0.0333mol•L-1 | D. | 0.1333 mol•L-1 |
 A、B、C、D、E、F为中学化学中的常见物质,且物质A由l~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题.
A、B、C、D、E、F为中学化学中的常见物质,且物质A由l~2种短周期元素组成,在一定条件下有如图转化关系,请完成下列问题.