题目内容
15.下列有关物质的性质与应用正确且相对应的是( )| A. | Na、K合金熔点低、沸点高,可用作原子反应堆导热液 | |
| B. | SiO2具有高沸点,可用作制备光导纤维 | |
| C. | NH3具有还原性,可用作制冷剂 | |
| D. | HF是强酸,可用于雕刻玻璃 |
分析 A.钠钾合金具有良好的导热性;
B.二氧化硅具有良好的光学特性;
C.液体氨气汽化吸收大量的热;
D.氢氟酸为弱酸.
解答 解:A.钠钾合金具有良好的导热性,可以用作原子反应堆导热液,故A正确;
B.二氧化硅具有良好的光学特性,可以制造光导纤维,与其熔点高性质无关,故B错误;
C.液体氨气汽化吸收大量的热,可用作制冷剂,与其还原性无关,故C错误;
D.氢氟酸为弱酸,能够与玻璃中的二氧化硅反应,能够雕刻玻璃,故D错误;
故选:A.
点评 本题考查了物质的用途,明确物质的性质是解题关键,侧重考查学生对基础知识掌握熟练程度,题目难度不大.

练习册系列答案
相关题目
5.从一种生产醋酸乙烯酯的废触媒(含醋酸锌、活性炭及少量有机物及氧化亚铁)中制取氯化锌中实验步骤如图
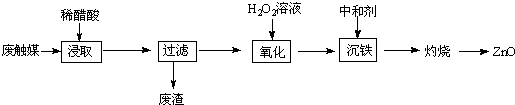
(1)浸取在三口烧瓶中进行,需给三口烧瓶加热并搅拌的目的是提高浸出速率和浸取率;浸出率随着浸取时间先增大后又减小,其原因是开始反应是加热搅拌加快浸出速率,但生成的醋酸锌被活性炭吸附,浸出率减小.
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是将吸附在活性炭孔内的醋酸锌全部释放出来.
(3)加入H2O2发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;沉铁需将溶液pH调整到约为5,最适宜的中和剂是bc(选填序号:a.石灰水 b.ZnO c.Zn.).
(4)高温灼烧时用到的硅酸盐质的仪器有酒精灯、坩埚和泥三角.
(5)某探究学习小组的同学拟利用废电池锌皮(主要成分为Zn,还含有少量的铁)制取氧化锌.如表列出了几种离子生成氢氧化物沉淀的pH:
实验中可选用的试剂:5mol•L-1HCl、2.0mol•L-1 HNO3、1.0mol•L-1 NaOH溶液.由废锌皮制ZnO的实验步骤依次为:向滤液中加入2.0mol•L-1 HNO3,使Fe2+转化完全为Fe3+,使其充分反应;滴加1.0mol•L-1NaOH,调节溶液PH约为5(或3.2≤pH<5.9),使Fe3+沉淀完全;向滤液中滴加1.0mol•L-1NaOH,调节溶液PH约为10(或8.9≤pH≤11),使Zn2+沉淀完全,再经过滤、洗涤、干燥;900℃煅烧.

(1)浸取在三口烧瓶中进行,需给三口烧瓶加热并搅拌的目的是提高浸出速率和浸取率;浸出率随着浸取时间先增大后又减小,其原因是开始反应是加热搅拌加快浸出速率,但生成的醋酸锌被活性炭吸附,浸出率减小.
(2)若先将废触媒在马弗炉中通氧气500℃处理一段时间,浸出率会大大提高,其原因是将吸附在活性炭孔内的醋酸锌全部释放出来.
(3)加入H2O2发生反应的离子方程式为H2O2+2Fe2++2H+=2Fe3++2H2O;沉铁需将溶液pH调整到约为5,最适宜的中和剂是bc(选填序号:a.石灰水 b.ZnO c.Zn.).
(4)高温灼烧时用到的硅酸盐质的仪器有酒精灯、坩埚和泥三角.
(5)某探究学习小组的同学拟利用废电池锌皮(主要成分为Zn,还含有少量的铁)制取氧化锌.如表列出了几种离子生成氢氧化物沉淀的pH:
| 开始沉淀的pH | 沉淀完全的pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
6.下列说法中正确的是( )
| A. | 1mol•L-1的NaCl溶液是指此溶液中含有1mol NaCl | |
| B. | 从1L0.5mol•L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol/L | |
| C. | 25℃时,1mol Cl2的体积约为22.4L | |
| D. | 1mol•L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol/L |
3.某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备: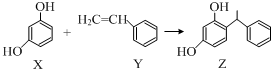
下列叙述错误的是( )

下列叙述错误的是( )
| A. | X、Y和Z均能使溴水褪色 | |
| B. | Y可作加聚反应单体,X可作缩聚反应单体 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | X和Z均能与Na2CO3溶液反应放出CO2 |
10.在密闭容器中A与B反应生成C,一段时间内其化学反应速率分别用v(A)、v(B)、v(C)表示.已知v(A)、v(B)、v(C)之间有以下关系2v(B)=v(A),v(C)=3v(B),则此反应可表示为( )
| A. | 2A+3B=2C | B. | A十3B=2C | C. | 2A+B=3C | D. | A+B=C |
20.如图实验操作或装置(略去部分夹持仪器)正确的是( )
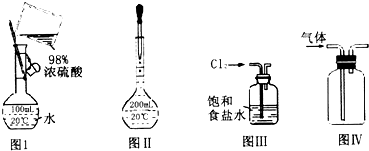

| A. | 图I表示为配制一定物质的量浓度稀硫酸时的操作 | |
| B. | 图Ⅱ表示为配制一定物质的量浓度的溶液定容时的操作 | |
| C. | 用图III所示装置吸收氯气中的氯化氢气体 | |
| D. | 用图IV所示装置收集一氧化氮气体 |
4.下列说法错误的是( )
| A. | 从1L1 mol•L-1的氯化钠溶液中取出10ml,其浓度仍是1mol•L-1 | |
| B. | 配制0.5L 10 mol•L-1的盐酸,需要氯化氢气体112L(标准状况) | |
| C. | 0.5 L 2 mol•L-1的氯化钡溶液中,钡离子和氯离子总数为1.806×1024 | |
| D. | 10g 98%硫酸(密度为1.84g/cm3)与10mL18.4 mol•L-1硫酸的浓度是不同的 |
5.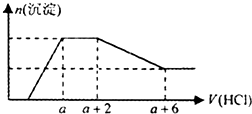 某溶液中可能含有SiO32-、OH-、CO32-、SO42-、AlO2-、HCO3-、Na+、Mg2+、Fe3+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示.下列说法正确的是( )
某溶液中可能含有SiO32-、OH-、CO32-、SO42-、AlO2-、HCO3-、Na+、Mg2+、Fe3+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示.下列说法正确的是( )
 某溶液中可能含有SiO32-、OH-、CO32-、SO42-、AlO2-、HCO3-、Na+、Mg2+、Fe3+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示.下列说法正确的是( )
某溶液中可能含有SiO32-、OH-、CO32-、SO42-、AlO2-、HCO3-、Na+、Mg2+、Fe3+、Al3+等离子.当向该溶液中逐滴加入一定物质的量浓度的盐酸溶液时,发现生成沉淀的物质的量随盐酸溶液的体积变化如图所示.下列说法正确的是( )| A. | 原溶液中一定含有Na2SO4 | |
| B. | 反应最后形成的溶液中的溶质只有NaCl | |
| C. | 原溶液中含有CO32-与AlO2- 的物质的量之比为1:2 | |
| D. | 原溶液中一定含有的阴离子是:OH-、CO32-、SiO32-、AlO2- |
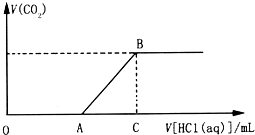 向200.0mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应.在上述所得溶液中,逐滴缓慢滴加2.0mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):
向200.0mL某物质的量浓度的NaOH溶液中缓慢通入一定量的CO2,充分反应.在上述所得溶液中,逐滴缓慢滴加2.0mol•L-1的盐酸,所得气体(不考虑溶解)的体积与滴加盐酸的体积关系如图(其中点A是线段OC上的动点):