题目内容
11.已知Co2O3在酸性溶液中易被还原成Co2+;则Co2O3、Cl2、FeCl3、I2的氧化性依次减弱.下列反应在水溶液中不可能发生的是( )| A. | Cl2+2FeCl2═2FeCl3 | B. | 3I2+6FeCl2═4FeCl3+2FeI3 | ||
| C. | Co2O3+6HCl═2CoCl2+Cl2↑+3H2O | D. | 2Fe3++2I-═2Fe2++I2 |
分析 根据化学方程式,只要根据氧化还原反应中氧化剂的氧化性强于氧化产物的氧化性得出的结果符合题干已知条件的,说明反应成立.
解答 解:A、根据反应Cl2+2FeCl2═2FeCl3,得出氧化性是:Cl2>FeCl3,和题意不相符合,不可能发生,故A不选;
B、根据反应:3I2+6FeCl2═4FeCl3+2FeI3,得出氧化性是:FeCl3<I2,和题意不相符合,反应不可能发生,故B选;
C、根据反应:Co2O3+6HCl=2CoCl2+Cl2↑+3H2O,得出氧化性是:Co2O3>Cl2,和题意相符合,反应可能发生,故C不选;
D、根据反应:2Fe3++2I-═2Fe2++I2,得出氧化性是:FeCl3<I2,和题意相符合,反应可能发生,故D不选.
故选B.
点评 本题考查学生分析和解决问题的能力,可以根据氧化剂的氧化性大于氧化产物的氧化性,难度不大.

练习册系列答案
相关题目
1.为减小CO2对环境的影响,在倡导“低碳”的同时,还需加强对CO2创新利用的研究.在T1℃时,将9molCO2和12molH2充入3L密闭容器中,发生反应CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0,容器中CH3OH的物质的量随时间变化如下图曲线I所示,平衡时容器内压强为P.改变某一条件重新进行上述反应,CH3OH的物质的量随时间变化如下图曲线Ⅱ所示.下列说法正确的是( )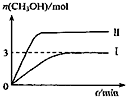

| A. | 曲线Ⅱ对应的条件改变是减小压强 | |
| B. | 若T2℃时,上述反应平衡常数为0.42,则T2<T1 | |
| C. | 在T1℃时,若起始时向容器中充入5 mol CO2、5 mol H2、5 mol CH3OH(g)和 5 mol H2O(g),则达平衡前v(正)>v(逆) | |
| D. | 在T1℃时,若起始时向容器中充入4.5molCO2、6mol H2,平衡时容器内压强P=$\frac{{P}_{1}}{2}$ |
2.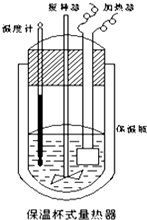 在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:
在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:
(1)试求CH3COOH的中和热△H=-53.3 kJ/mol.
(2)CH3COOH的中和热的文献值为56.1KJ•mol-1,则请你分析在(1)中测得的实验值偏差可能的原因①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等.
(3)实验中NaOH过量的目的是使碱稍稍过量,为了能保证CH3COOH溶液完全被中和,从而提高实验的准确度.
(4)CH3COOH的中和热与盐酸的中和热绝对值相比,HCl的较大,原因是CH3COOH是弱酸,只是少部分电离,CH3COOH发生电离时要吸热.
 在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:
在如图所示的量热计中,将100mL0.50mol•L CH3COOH溶液 与100mL0.55mol•L-1NaOH溶液混合.已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J•℃-1,生成溶液的比热容为4.184J•g-1•℃-1,溶液的密度均近似为1g•mL-1.实验中某同学计算中和热,记录数据如下:| 实验序号 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 醋酸溶液 | 氢氧化钠溶液 | 混合溶液 | |
| 1 | 25.0 | 25.1 | 27.8 |
| 2 | 25.1 | 25.3 | 27.9 |
| 3 | 25.2 | 25.5 | 28.0 |
(2)CH3COOH的中和热的文献值为56.1KJ•mol-1,则请你分析在(1)中测得的实验值偏差可能的原因①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等.
(3)实验中NaOH过量的目的是使碱稍稍过量,为了能保证CH3COOH溶液完全被中和,从而提高实验的准确度.
(4)CH3COOH的中和热与盐酸的中和热绝对值相比,HCl的较大,原因是CH3COOH是弱酸,只是少部分电离,CH3COOH发生电离时要吸热.
19.下列反应属于加成反应的是( )
| A. | CH2=CH2+H-OH$\stackrel{催化剂}{→}$ CH3CH2OH | |
| B. | H2+Cl2$\frac{\underline{\;光照\;}}{\;}$ 2HCl | |
| C. | CH3CH2Br+KOH$→_{△}^{H_{2}O}$CH3CH2OH+KBr | |
| D. | CH3CH3+2Cl2 $\stackrel{光}{→}$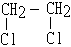 +2HCl +2HCl |
6.下列说法中正确的是( )
| A. | 1mol•L-1的NaCl溶液是指此溶液中含有1mol NaCl | |
| B. | 从1L0.5mol•L-1的NaCl溶液中取出100mL溶液,其物质的量浓度变为0.1mol/L | |
| C. | 25℃时,1mol Cl2的体积约为22.4L | |
| D. | 1mol•L-1的CaCl2溶液中,Cl-的物质的量浓度为2 mol/L |
3.某化妆品的组分Z具有美白功效,原从杨树中提取,现可用如下反应制备: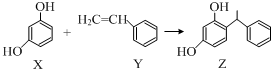
下列叙述错误的是( )

下列叙述错误的是( )
| A. | X、Y和Z均能使溴水褪色 | |
| B. | Y可作加聚反应单体,X可作缩聚反应单体 | |
| C. | Y既能发生取代反应,也能发生加成反应 | |
| D. | X和Z均能与Na2CO3溶液反应放出CO2 |
20.如图实验操作或装置(略去部分夹持仪器)正确的是( )
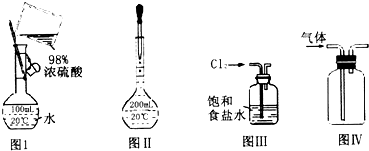

| A. | 图I表示为配制一定物质的量浓度稀硫酸时的操作 | |
| B. | 图Ⅱ表示为配制一定物质的量浓度的溶液定容时的操作 | |
| C. | 用图III所示装置吸收氯气中的氯化氢气体 | |
| D. | 用图IV所示装置收集一氧化氮气体 |
1.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 在常温常压下,11.2L N2含有的分子数为NA | |
| B. | 标准状况下,18g H2O所占的体积约是22.4L | |
| C. | 32gO2在标准状况下所占的体积约为22.4L | |
| D. | 1mol Ne中约含有6.02×1024个电子 |