题目内容
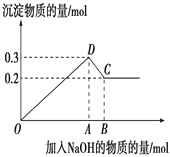
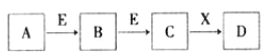
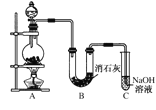
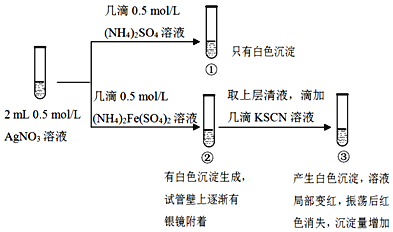
【题目】某强酸性溶液X中可能含有Fe2+、Al3+、NH4+、CO32-、SO42-、Cl-中的若干种,现取X溶液进行实验,实验过程及产物如图。下列说法正确的是( )
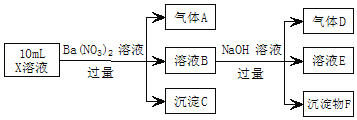
A.A是一种无色、无毒的气体
B.沉淀F为![]()
C.实验室可用排水法收集气体D
D.往溶液E中通入少量![]() ,有沉淀产生
,有沉淀产生
【答案】D
【解析】
强酸性溶液含大量的氢离子,一定不会存在CO32-,结合实验流程可知,加入过量硝酸钡生成沉淀,则该沉淀C为BaSO4,说明溶液中含有SO42-离子,生成气体A,因酸性条件下硝酸根离子具有强氧化性,可以和还原性的离子发生反应生成NO气体,所以溶液一定含Fe2+离子;溶液B中加入过量NaOH溶液,生成气体D,则D为NH3,说明溶液中含有NH4+离子,沉淀物F为Fe(OH)3,溶液E中含NaOH、硝酸钡,且E中可能含偏铝酸钠,据此分析解答。
由上述分析可知,X中一定含Fe2+、NH4+、SO42-,可能含A13+、C1-,一定不含CO32-。
A.A为NO,为无色有毒气体,故A错误;
B.由3Fe2++NO3-+4H+=3Fe3++NO↑+2H2O,B中含氧化还原反应生成的铁离子,与NaOH反应生成F为Fe(OH)3,故B错误;
C.D为氨气,极易溶于水,不能用排水法收集,故C错误;
D.E中含NaOH、硝酸钡,可能含偏铝酸钠,通入二氧化碳一定发生CO2+2OH-+Ba2+=BaCO3↓+H2O,可能发生2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-,则往溶液E中通入少量CO2,有沉淀产生,故D正确;
故选D。

 全优点练单元计划系列答案
全优点练单元计划系列答案【题目】合成氨原料可以由天然气制取。其主要反应为:CH4(g)+H2O(g)→CO(g)+3H2(g)
(1)1 m3(标准状况)CH4按上式完全反应,产生H2_________mol。(精确到0.1)
(2)CH4和O2的反应为:2CH4(g)+O2(g)→2CO(g)+4H2(g)
设CH4同时和H2O(g)及O2(g)反应。1 m3(标准状况)CH4按上述两式完全反应,产物气体的体积V m3(标准状况)的取值范围为________。
(3)CH4和H2O(g)及富氧空气(O2含量较高的空气)混合反应,产物气体组成如下表:
气体 | CO | H2 | N2 | O2 |
体积(L) | 25 | 60 | 15 | 2.5 |
计算该富氧空气中O2和N2的体积比,V(O2):V(N2)=________。
(4)若CH4和H2O(g)及(3)题中的富氧空气混合反应,产物气体中V(H2):V(N2)=3:1(合成氨反应的最佳比),则反应中的H2O(g)和富氧空气的体积比为_______。