题目内容
【题目】贝诺酯是解热镇痛抗炎药,其结构如图所示。下列有关说法正确的是
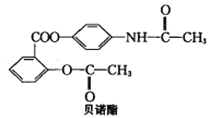
A. 分子式为C17H14O5N
B. 贝诺酯能发生银镜反应
C. 1 mol贝诺酯与H2发生加成反应最多消耗8mol H2
D. 在氢氧化钠水溶液中水解可以得到3种有机物钠盐
【答案】D
【解析】A.由C、H、O、N等几种元素组成的有机物的分子中,若N原子数为奇数,则H原子数也一定是奇数,A不正确; B. 贝诺酯分子中没有醛基,其不能发生银镜反应,B不正确;C. 1 mol贝诺酯与H2发生加成反应不可能消耗8mol H2,因为酯类物质不能与氢气发生加成反应,C不正确;D. 贝诺酯在NaOH溶液中水解,酯基与酰胺键断裂可得乙酸钠、对氨基苯酚钠与![]() 等三种有机物钠盐,D正确。本题选D。
等三种有机物钠盐,D正确。本题选D。

练习册系列答案
相关题目