题目内容
16.下说法错误的是( )| A. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| B. | 化学变化中的能量变化主要是由于化学键变化引起的 | |
| C. | 能量变化是化学反应的基本特征之一 | |
| D. | 各种物质都储存有化学能,物质的组成、结构不同,所包含的化学能也不同 |
分析 A.化学反应中的能量变化的大小与反应物的质量成正比;
B.化学变化中的能量变化主要是由化学键的断裂和形成引起的;
C.所有化学反应均伴随着能量变化;
D.原子内部和原子间均含有能量.
解答 解:A.化学反应中的能量变化的大小与反应物的质量成正比,故A错误;
B.断裂化学键要吸收能量,形成化学键要放出能量,化学变化中的能量变化主要是由化学键的断裂和形成引起的,故B正确;
C.所有化学反应均伴随着能量变化,故能量变化是化学反应的基本特征之一,故C正确;
D.原子内部和原子间均含有能量,所以各种物质都储存有化学能,组成、结构不同,所包含的化学能也不同,故D正确.
故选A.
点评 本题考查化学反应的基本特征和能量变化的原因,注意化学反应必然伴随着能量变化.

练习册系列答案
相关题目
7.使用氢氧燃料电池的汽车已在北京街头出现.下列有关该氢氧燃料电池的说法中,正确的是( )
| A. | H2在正极发生氧化反应 | |
| B. | 供电时的总反应是 2H2+O2 $\frac{\underline{\;点燃\;}}{\;}$ 2H2O | |
| C. | 氢氧燃料电池中反应放出的热量转变为电能 | |
| D. | 产物是无污染的水,属于环境友好电池 |
1.下列说法正确的是( )
| A. | F、Cl、Br、I最高价氧化物对应水化物的酸性依次减弱 | |
| B. | 多电子原子中,在离核较近的区域内运动的电子能量较高 | |
| C. | 元素原子的最外层电子数等于元素的最高化合价 | |
| D. | Na、Mg、Al失电子能力和最高价氧化物对应水化物的碱性均依次减弱 |
8.下列物质 ①乙烷 ②乙炔 ③甲苯 ④苯 ⑤聚乙烯 ⑥乙醇,其中既能与溴水反应又能与酸性高锰酸钾溶液反应的是( )
| A. | ②③④⑤ | B. | ②⑤⑥ | C. | ② | D. | ②⑤ |
5.在图所示的原电池中,下列说法正确的是( )
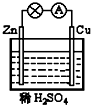

| A. | 正极反应为 Cu-2e-Cu2+ | B. | 溶液中H+向锌片移动 | ||
| C. | 电子由锌片通过导线流向铜 | D. | 该装置能将电能转化为化学能 |
6.将1mol甲烷和适量的Cl2混合后光照,充分反应后生成CH3Cl、CH2Cl2、CHCl3、CCl4四种有机产物的物质的量依次增大0.1mol,则参加反应的Cl2的物质的量为( )
| A. | 1.5mol | B. | 3mol | C. | 4.5mol | D. | 6mol |
 在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示:
在一体积为10L的容器中,通入一定量的CO和H2O,850℃时发生反应:CO(g)+H2O(g)?CO2(g)+H2(g).CO和H2O浓度变化如图所示: 氮是地球上极为丰富的元素.
氮是地球上极为丰富的元素.