题目内容
5.在图所示的原电池中,下列说法正确的是( )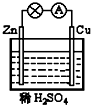
| A. | 正极反应为 Cu-2e-Cu2+ | B. | 溶液中H+向锌片移动 | ||
| C. | 电子由锌片通过导线流向铜 | D. | 该装置能将电能转化为化学能 |
分析 该原电池中,锌为负极易失电子发生氧化反应,铜为正极溶液中的氢离子在正极得电子发生还原反应,电子从负极沿导线流向正极,阳离子移向正极,以此解答该题.
解答 解:A、锌比铜活泼,形成原电池时锌为负极,铜为正极溶液中的氢离子在正极得电子发生还原反应,反应式2H++2e-=H2↑,故A错误;
B、该原电池中,阳离子移向正极,所以H+向铜片移动,故B错误;
C、电子由负极锌片通过导线流向正极铜片,故C正确;
D、原电池将化学能转化为电能,故D错误.
故选C.
点评 本题考查了原电池原理,为高频考点,侧重于学生的分析能力的考查,明确正负极上得失电子、电子流向即可解答,难度不大.

练习册系列答案
 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案
相关题目
15.为探究 Na、Mg、Al的金属性强弱顺序,某课外小组同学进行了如下实验:
(1)请在下表中填写与实验步骤对应的实验现象序号:
(2)写出钠与水反应的离子方程式2Na+2H2O=2Na++2OH-+H2↑.
(3)该实验得出的结论是Na、Mg、Al的金属活动性顺序由强到弱.
(4)用原子结构理论解释上述实验结论:同周期元素从左至右原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐减小(填“增大”或“减小”),原子核对核外电子的引力逐渐增强,失电子能力逐渐减弱(填“增强”或“减弱”),因此金属性逐渐减弱(填“增强”或“减弱”).
| 实验步骤 | 1.将一小块金属钠放入滴有酚酞溶液的冷水中 2.将一小段用砂纸打磨后的镁带放入试管中,加入少量水,加热至水沸腾,冷却后,向试管中滴加酚酞溶液 3.将一小段镁带投入稀盐酸中 4.将一小片铝投入稀盐酸中 |
| 实验现象 | ①剧烈反应,迅速生成大量的气体 ②浮在水面上,熔成小球,不断游动,小球渐小最终消失,溶液变红 ③反应不剧烈,产生无色气体 ④有气体产生,溶液变成红色 |
| 实验步骤 | 1 | 2 | 3 | 4 |
| 实验现象 |
(3)该实验得出的结论是Na、Mg、Al的金属活动性顺序由强到弱.
(4)用原子结构理论解释上述实验结论:同周期元素从左至右原子的电子层数相同,核电荷数逐渐增多,原子半径逐渐减小(填“增大”或“减小”),原子核对核外电子的引力逐渐增强,失电子能力逐渐减弱(填“增强”或“减弱”),因此金属性逐渐减弱(填“增强”或“减弱”).
16.下说法错误的是( )
| A. | 化学反应中能量变化的大小与反应物的质量多少无关 | |
| B. | 化学变化中的能量变化主要是由于化学键变化引起的 | |
| C. | 能量变化是化学反应的基本特征之一 | |
| D. | 各种物质都储存有化学能,物质的组成、结构不同,所包含的化学能也不同 |
13.下列物质各组物质中不能全部发生加成反应的是( )
| A. | 氯乙烯、溴乙烯 | B. | 乙烯、乙炔 | C. | 乙烷、乙烯 | D. | 苯、2-丁烯 |
17.下列各组物质中,可以用分液漏斗分离的是( )
| A. | 液溴和溴苯 | B. | 溴苯和苯 | C. | 硝基苯和水 | D. | 苯和硝基苯 |
15.钡盐行业生产中排出大量的钡泥 主要含有【BaCO3、BaSiO3、BaSO3、Ba(FeO2)2】等.某主要生产BaCl2、BaCO3、BaSO4的化工厂利用钡泥制取Ba(NO3)2,其部分工艺流程如下
已知部分离子沉淀所需的pH如下表
问答下列问题
(1)上述③过滤操作中除要用到玻璃棒,铁架台,烧杯等还缺的玻璃仪器有漏斗,废渣中的主要化学物质是BaSiO3、H2SiO3、Fe(OH)3、BaSO4(写化学式)
(2)写出酸溶过程中涉及氧化还原反应的离子方程式3BaSO3+2H++2NO3-=3BaSO4+2NO↑+H2O
(3)该厂结合本厂实际,选用的X为BaCO3(填化学式);中和Ⅰ使溶液中Fe3+、H+(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)
(4)上述④洗涤的目的是减少废渣中可溶性钡盐对环境的污染.
(5)由于废渣给周围环境造成了一定的污染,该工厂想设计一个方案,将工厂废渣进行分离,并制备生产光导纤维的主要原材料,请你按示例简要设计实验分案(示例:取物质A$\stackrel{加热}{→}$$\stackrel{蒸发}{→}$ 得到物质B)
废渣$\stackrel{适量氢氧化钾}{→}$$\stackrel{搅拌过滤}{→}$滤液$\stackrel{加入足量盐酸}{→}$$\stackrel{搅拌过滤}{→}$$\stackrel{加热}{→}$二氧化硅.

已知部分离子沉淀所需的pH如下表
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 4.7 | 7.5 | 1.4 |
| 沉淀完全pH | 6.7 | 14 | 3.7 |
(1)上述③过滤操作中除要用到玻璃棒,铁架台,烧杯等还缺的玻璃仪器有漏斗,废渣中的主要化学物质是BaSiO3、H2SiO3、Fe(OH)3、BaSO4(写化学式)
(2)写出酸溶过程中涉及氧化还原反应的离子方程式3BaSO3+2H++2NO3-=3BaSO4+2NO↑+H2O
(3)该厂结合本厂实际,选用的X为BaCO3(填化学式);中和Ⅰ使溶液中Fe3+、H+(填离子符号)的浓度减少(中和Ⅰ引起的溶液体积变化可忽略)
(4)上述④洗涤的目的是减少废渣中可溶性钡盐对环境的污染.
(5)由于废渣给周围环境造成了一定的污染,该工厂想设计一个方案,将工厂废渣进行分离,并制备生产光导纤维的主要原材料,请你按示例简要设计实验分案(示例:取物质A$\stackrel{加热}{→}$$\stackrel{蒸发}{→}$ 得到物质B)
废渣$\stackrel{适量氢氧化钾}{→}$$\stackrel{搅拌过滤}{→}$滤液$\stackrel{加入足量盐酸}{→}$$\stackrel{搅拌过滤}{→}$$\stackrel{加热}{→}$二氧化硅.

 ;G的结构简式HCOOCH3;
;G的结构简式HCOOCH3; .写出D与C反应生成A的化学方程式CH3OH+
.写出D与C反应生成A的化学方程式CH3OH+ +H2O.
+H2O.