题目内容
3.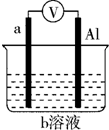 如图是某同学设计的一个简易的原电池装置,回答下列问题.
如图是某同学设计的一个简易的原电池装置,回答下列问题.(1)若a为镁、b为CuCl2,则正极材料为Al,负极上的电极反应式为Mg-2e-═Mg2+.
(2)若a为镁、b为NaOH,则Mg极上发生还原反应(填“氧化”或“还原”),负极上的电极反应式为Al-3e-+4OH-═AlO2-+2H2O.
(3)若a为铜、b为浓硝酸,则电流的方向为铝→铜(填电极材料),正极上的电极反应式为2H++NO3-++e-═H2O+NO2↑,.
(4)上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑电解质溶液的性质.
分析 (1)若a为镁、b为CuCl2,则镁比铝活泼,负极为镁发生氧化反应,正极材料为铝发生还原反应;
(2)若a为镁、b为NaOH,则铝在碱中比镁活泼,负极为铝发生氧化反应,正极材料为镁发生还原反应;
(3)若a为铜、b为浓硝酸,铝与浓硝酸发生钝化,则铜为负极发生氧化反应,铝为正极发生还原反应,电流的方向为正极到负极;
(4)上述上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑电解质溶液的性质.
解答 解:(1)若a为镁、b为CuCl2,则镁比铝活泼,负极为镁发生氧化反应,反应式为:Mg-2e-═Mg2+,正极材料为铝发生还原反应,故答案为:Al;Mg-2e-═Mg2+;
(2)若a为镁、b为NaOH,则铝在碱中比镁活泼,负极为铝发生氧化反应,反应式为:Al-3e-+4OH-═AlO2-+2H2O,正极材料为镁发生还原反应,故答案为:还原;Al-3e-+4OH-═AlO2-+2H2O;
(3)若a为铜、b为浓硝酸,铝与浓硝酸发生钝化,则铜为负极发生氧化反应,铝为正极发生还原反应反应式为:2H++NO3-++e-═H2O+NO2↑,电流的方向为正极铝到负极铜,故答案为:铝,铜;2H++NO3-++e-═H2O+NO2↑;
(4)上述上述事实表明,确定原电池中电极的正负时,不仅要考虑电极材料本身的性质,还要考虑电解质溶液的性质,故答案为:电解质溶液的性质.
点评 本题考查原电池的组成和工作原理,题目难度不大,注意把握以镁、铝为电极材料,电解质溶液的酸碱性不同,电极反应不同,为易错点.

练习册系列答案
相关题目
13.下表是元素周期表的一部分,回答下列有关问题:
(1)写出下列元素符号:①N,⑥Si,⑦S.
(2)在①-(12)元素中,金属性最强的元素是K,非金属性最强的元素是F,最不活泼的元素是Ar.(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是BD.
A.常温下⑦的单质和⑧的单质状态不同
B.⑧的氢化物比⑦的氢化物稳定
C.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
D.⑧的最高价氧化物的水化物的酸性比⑦的最高价氧化物的水化物的酸性强.
| 族 周期 | IA | ⅡA | ⅢA | IVA | VA | VIA | VⅡA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| 4 | ⑩ | (11) | (12) |
(2)在①-(12)元素中,金属性最强的元素是K,非金属性最强的元素是F,最不活泼的元素是Ar.(均填元素符号)
(3)元素⑦与元素⑧相比,非金属性较强的是Cl(用元素符号表示),下列表述中能证明这一事实的是BD.
A.常温下⑦的单质和⑧的单质状态不同
B.⑧的氢化物比⑦的氢化物稳定
C.一定条件下⑦和⑧的单质都能与氢氧化钠溶液反应
D.⑧的最高价氧化物的水化物的酸性比⑦的最高价氧化物的水化物的酸性强.
18.X、Y、Z、M、N代表五种金属,有以下化学反应:
(1)水溶液中X+Y2+═X2++Y;
(2)Z+2H2O(冷水)═Z(OH)2+H2↑;
(3)M、N为电极,与N盐溶液组成原电池,M电极反应为M-2e-═M2+;
(4)Y可以溶于稀硫酸中,M不被稀硫酸氧化.
则这五种金属的活动性由弱到强的顺序是( )
(1)水溶液中X+Y2+═X2++Y;
(2)Z+2H2O(冷水)═Z(OH)2+H2↑;
(3)M、N为电极,与N盐溶液组成原电池,M电极反应为M-2e-═M2+;
(4)Y可以溶于稀硫酸中,M不被稀硫酸氧化.
则这五种金属的活动性由弱到强的顺序是( )
| A. | M<N<Y<X<Z | B. | N<M<X<Y<Z | C. | N<M<Y<X<Z | D. | X<Z<N<M<Y |
8.如图所示装置是化学实验室中的常用装置,它有多种用途,以下各项用途和操作都正确的是( )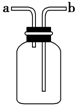

| A. | 洗气装置:瓶内放一定体积溶液,由a管口进气 | |
| B. | 收集不溶于水的气体:瓶内充满水,由b管口进气 | |
| C. | 排空气法收集氧气:由a管口进气 | |
| D. | 排空气法收集氢气:由a管口进气 |
12.Ⅰ煤化工中常需研究不同温度下平衡常数、投料比等问题.
已知:CO (g)+H2O (g)?H2 (g)+CO2 (g)平衡常数K随温度的变化如下表:
回答下列问题
(1)该反应的平衡常数表达式K=$\frac{c({H}_{2})•c(C{O}_{2})}{c(CO)•c({H}_{2}0)}$,△H=<0(填“<”、“>”、“=”)
(2)已知在一定温度下,C(s)+CO2 (g)?2CO (g)平衡常数K1
C(s)+H2O (g)?H2 (g)+CO (g)平衡常数K2,
则K、K1、K2,之间的关系是K=$\frac{{K}_{2}}{{K}_{1}}$
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为80%;若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,此时v正=v逆 (填“>”、“=”或“<”).
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
Ⅱ(4)已知:KMnO4+H2C2O4+H2SO4→MnSO4+K2SO4+CO2↑+H20(未配平),向酸性KMnO4溶液中加入一定量的H2C2O4溶液,当溶液中的KMnO4耗尽后,紫色溶液将褪去.为确保能观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5.
(5)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案
表中x=2 ml,理由是保证其它条件不变,只改变H2C2O4的浓度,从而达到对比的目的.
已知:CO (g)+H2O (g)?H2 (g)+CO2 (g)平衡常数K随温度的变化如下表:
| 温度/℃ | 400 | 500 | 800 |
| 平衡常数K | 9.94 | 9 | 1 |
(1)该反应的平衡常数表达式K=$\frac{c({H}_{2})•c(C{O}_{2})}{c(CO)•c({H}_{2}0)}$,△H=<0(填“<”、“>”、“=”)
(2)已知在一定温度下,C(s)+CO2 (g)?2CO (g)平衡常数K1
C(s)+H2O (g)?H2 (g)+CO (g)平衡常数K2,
则K、K1、K2,之间的关系是K=$\frac{{K}_{2}}{{K}_{1}}$
(3)800℃时,向一个10L的恒容反应器中充入0.40molCO和1.60mol水蒸气,经一段时 间后反应达到平衡,此时CO的转化率为80%;若保持其他条件不变,向平衡体系中再通入0.10molCO和0.40mol CO2,此时v正=v逆 (填“>”、“=”或“<”).
某小组利用H2C2O4溶液和酸性KMnO4溶液反应来探究“条件对化学反应速率的影响”.
Ⅱ(4)已知:KMnO4+H2C2O4+H2SO4→MnSO4+K2SO4+CO2↑+H20(未配平),向酸性KMnO4溶液中加入一定量的H2C2O4溶液,当溶液中的KMnO4耗尽后,紫色溶液将褪去.为确保能观察到紫色褪去,H2C2O4与KMnO4初始的物质的量需要满足的关系为n(H2C2O4):n(KMnO4)≥2.5.
(5)为探究反应物浓度对化学反应速率的影响,该小组设计了如下实验方案
| 实验序号 | 反应温度/℃ | H2C2O4溶液 | 酸性KMO4溶液 | H2O | ||
| V/mL | c/(mol•L-1) | V/mL | c/(mol•L-1) | V/mL | ||
| ① | 25 | 8.0 | 0.20 | 5.0 | 0.010 | 0 |
| ② | 25 | 6.0 | 0.20 | 5.0 | 0.010 | x |
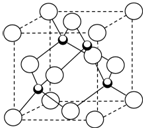 原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.
原子序数小于36的X、Y、Z、W四种元素,其中X是形成化合物种最多的元素,Y原子基态时最外层电子数是其内层电子数的2倍,Z原子基态时2p原子轨道上有3个未成对的电子,W的原子序数为29.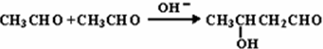
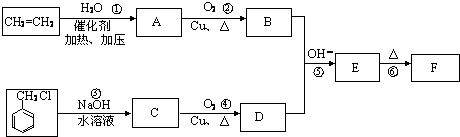
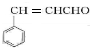 .E中含氧官能团的名称为醛基、羟基.
.E中含氧官能团的名称为醛基、羟基.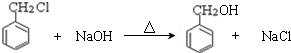
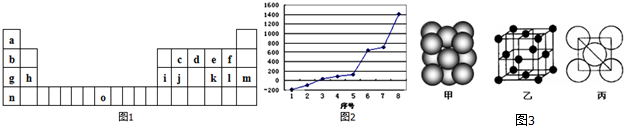
 ,它在常温下呈液态,形成晶体时,属于
,它在常温下呈液态,形成晶体时,属于