题目内容
15.已知两个醛分子在NaOH溶液作用下可以发生加成反应,生成一种羟基醛: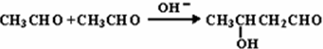
肉桂醛F(分子式为C9H8O)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如下路线合成的
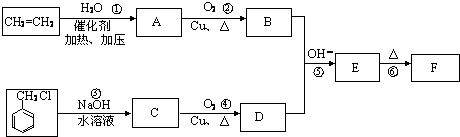
已知:反应⑥为含羟基的物质在浓硫酸催化作用下分子内脱水的反应.反
应⑤为碱性条件下醛醛加成反应,请回答
(1)肉桂醛F的结构简式为:
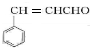 .E中含氧官能团的名称为醛基、羟基.
.E中含氧官能团的名称为醛基、羟基.(2)写出下列转化的化学方程式:
②2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
③
写出有关反应的类型:①加成④氧化.
(3)符合下列要求的E物质的同分异构体有3种(苯环上有两个取代基,其中有一个甲基在对位且属于酯类).
分析 乙烯与水发生加成反应生成A为C2H5OH,A发生催化氧化生成B为CH3CHO,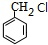 发生水解反应生成C为
发生水解反应生成C为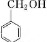 ,C发生催化氧化生成D为
,C发生催化氧化生成D为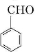 ,B与D发生醛的加成反应生成E为
,B与D发生醛的加成反应生成E为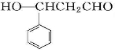 ,E在浓硫酸、加热条件下发生消去反应生成F为
,E在浓硫酸、加热条件下发生消去反应生成F为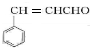 ,据此分析解答.
,据此分析解答.
解答 解:乙烯与水发生加成反应生成A为C2H5OH,A发生催化氧化生成B为CH3CHO, 发生水解反应生成C为
发生水解反应生成C为 ,C发生催化氧化生成D为
,C发生催化氧化生成D为 ,B与D发生醛的加成反应生成E为
,B与D发生醛的加成反应生成E为 ,E在浓硫酸、加热条件下发生消去反应生成F为
,E在浓硫酸、加热条件下发生消去反应生成F为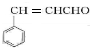 ,
,
(1)F结构简式为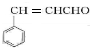 ,E为
,E为 ,E中含氧官能团名称是醛基、醇羟基,
,E中含氧官能团名称是醛基、醇羟基,
故答案为: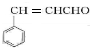 ;羟基、醛基;
;羟基、醛基;
(2)②为乙醇的催化氧化反应,反应方程式为2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
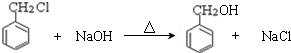
③为1-氯甲苯的水解反应,生成苯甲醇和NaCl,反应方程式为 ,
,
①④反应类型分别是加成反应、氧化反应,
故答案为:2C2H5OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O; ;
;
加成;氧化;
(3)E为 ,E的同分异构体符合下列条件:苯环上有两个取代基,其中有一个甲基在对位且属于酯类,有对甲基苯甲酸甲酯、对甲基甲酸苯甲酯、对甲基乙酸苯酯,所以有3种,
,E的同分异构体符合下列条件:苯环上有两个取代基,其中有一个甲基在对位且属于酯类,有对甲基苯甲酸甲酯、对甲基甲酸苯甲酯、对甲基乙酸苯酯,所以有3种,
故答案为:3.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力及知识迁移能力,根据反应条件结合题给信息进行推断,正确推断各物质结构简式是解本题关键,知道常见反应类型及反应条件,易错点是:(3)中对甲基乙酸苯酯易漏掉而导致错误.

练习册系列答案
相关题目
5.下列对有机物结构或性质的描述,错误的是( )
| A. | 一定条件下,Cl2 可在甲苯的苯环或侧链上发生取代反应? | |
| B. | 苯酚钠溶液中通入CO2 生成苯酚,则碳酸的酸性比苯酚弱? | |
| C. | 乙烷和丙烯混合气体的物质的量共1 mol,完全燃烧生成3 mol H2O | |
| D. | 光照下,2,2-二甲基丙烷与Br2 反应其一溴取代物只有一种 |
10.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2 L水中含有分子的数目为0.5NA | |
| B. | 1 mol Cl2与足量的NaOH溶液反应,转移的电子数为1NA | |
| C. | 100 mL 0.2 mol•L-1的FeCl3溶液中,含Fe3+数为0.02NA | |
| D. | 常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子 |
7.最近美国宇航局(NASA)马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”-全氟丙烷(C3F8),并提出用其“温室化火星”使其成为第二个地球的计划.有关全氟丙烷的说法正确的是( )
| A. | 全氟丙烷不能使溴水褪色 | |
| B. | 全氟丙烷的电子式为: | |
| C. | 相同压强下,沸点:C3F8<C3H8 | |
| D. | 分子中三个碳原子可能处于同一直线上 |
4.由碳的氧化物直接合成乙醇燃料已进入大规模生产.如图是由二氧化碳合成乙醇的技术流程:
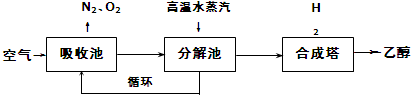
吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇.回答下列问题:
(1)写出吸收池中反应的离子方程式CO2+CO32-+H2O=2HCO3-.
(2)从分解池中循环使用的物质是K2CO3.
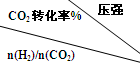
(3)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如表:
提高氢碳n(H2)/n(CO2)比,对生成乙醇有利(选填“不利”、“有利”或“无影响”).

吸收池中盛有饱和碳酸钾溶液,把含有二氧化碳的空气吹入吸收池中,吸收池中反应液进入分解池后,向分解池中通入高温水蒸汽,把二氧化碳从溶液中提取出来,在合成塔中和氢气经化学反应使之变为可再生燃料乙醇.回答下列问题:
(1)写出吸收池中反应的离子方程式CO2+CO32-+H2O=2HCO3-.
(2)从分解池中循环使用的物质是K2CO3.
(3)在一定压强下,测得由CO2制取CH3CH2OH的实验数据如表:
 | 500 | 600 | 700 | 800 |
| 1.5 | 45 | 33 | 20 | 12 |
| 2.0 | 60 | 43 | 28 | 15 |
| 3.0 | 83 | 62 | 37 | 22 |
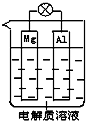 一种原电池的组成如图所示.试回答下列问题(灯泡功率合适):
一种原电池的组成如图所示.试回答下列问题(灯泡功率合适):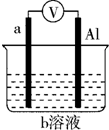 如图是某同学设计的一个简易的原电池装置,回答下列问题.
如图是某同学设计的一个简易的原电池装置,回答下列问题.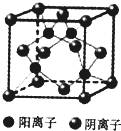 T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增.已知:
T、X、Y、Z、Q、R、W为周期表前四周期元素,原子序数依次递增.已知: