题目内容
甲容器中发生了某化学反应,测得反应过程中,容器中存在Na+、H2O、CN-、ClO-、HCO3-、N2、Cl-七种粒子,其中ClO-和N2的物质的量随时间变化的曲线如图所示。根据题意完成下列填空: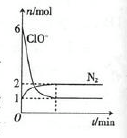
(1)CN一中氮元素的化合价是 。
(2)甲容器中发生反应的离子方程式是 。该反应的氧化产物是 (填化学式)。
(3)乙容器中用ClO2代替ClO-,溶液呈碱性,若最终两容器中N2的物质的量相同。则甲、乙两容器中参加反应的氧化剂的物质的量之比为 。
(1)-3
(2)5ClO-+2CN-+H2O=N2↑+2HCO3-+5Cl-(写可逆符号也给分);N2、HCO3-
(3)5∶2(每空2分)
解析试题分析:(1)非金属性C<N,所以氮元素的化合价是-3
(2)根据题意:5ClO-+2CN-+H2O=N2↑+2HCO3-+5Cl-(写可逆符号也给分);该反应的氧化产物是N2、HCO3-
(3)最终都被还原为Cl-,ClO2得5个电子,ClO-得2个电子,若最终两容器中N2的物质的量相同。则甲、乙两容器中参加反应的氧化剂的物质的量之比为5∶2。
考点:考察化合价确定、离子方程式、化学反应的计算。

练习册系列答案
 快乐小博士巩固与提高系列答案
快乐小博士巩固与提高系列答案
相关题目
在Na+浓度为0.5mol/L的某澄清溶液中,还可能含有下表中的若干种离子:
| 阳离子 | K+、Ag+、Mg2+、Ba2+ |
| 阴离子 | NO3-、CO32-、SiO32-、SO42- |
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 向该溶液中加入足量稀HCl | 产生白色沉淀并放出0.56L气体 |
| Ⅱ | 将Ⅰ的反应混合液过滤,对沉淀洗涤、灼烧至恒重,称量所得固体质量 | 固体质量为2.4g |
| Ⅲ | 在Ⅱ的滤液中滴加BaC12溶液 | 无明显现象 |
(1)实验I能确定一定不存在的阳离子是 。
(2)实验I中生成沉淀的离子方程式为 。
(3)通过实验I、Ⅱ、Ⅲ和必要计算,填写下表中阴离子的浓度(能计算出的,填写计算结果,一定
不存在的离子填“0”,不能确定是否存在的离子填“?”)
| 阴离子 | NO3- | CO32- | SiO32- | SO42- |
| c/mol·L-1 | | | | |

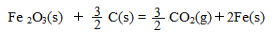 △H = +230 kJ/mol
△H = +230 kJ/mol