题目内容
【题目】下列说法正确的是
A. 恒容密闭容器中进行的反应:A(s)+3B(g)![]() 2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
2C(g)+D(g),如果气体密度保持不变,说明反应已经达到平衡
B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
CO ( g) + H2 (g),其他条件不变,缩小容器体积,正速率减小,逆速率增大
C. N2(g) + 3H2(g)![]() 2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
2NH3(g) △H=—93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,可以放出37.2 kJ的热量
D. A(g)+ 3B (g) ![]() 2C (g) + D (g),在两种不同情况下的反应速率分别为:①
2C (g) + D (g),在两种不同情况下的反应速率分别为:①![]() ,②
,②![]() ,则前者比后者快
,则前者比后者快
【答案】A
【解析】
A. 恒容密闭容器中进行的反应:A(s)+3B(g)![]() 2C(g)+D(g),因为A为固体,所以如果气体密度保持不变,说明反应已经达到平衡,故A正确;B. C ( s) + H2O (g)
2C(g)+D(g),因为A为固体,所以如果气体密度保持不变,说明反应已经达到平衡,故A正确;B. C ( s) + H2O (g) ![]() CO ( g) + H2 (g),其他条件不变,缩小容器体积,压强增大,正、逆速率均增大,故B错误;C. N2(g) + 3H2(g)
CO ( g) + H2 (g),其他条件不变,缩小容器体积,压强增大,正、逆速率均增大,故B错误;C. N2(g) + 3H2(g)![]() 2NH3(g) △H=-93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,由于是可逆反应,因此放出的热量小于37.2 kJ ,故C错误;D. 根据化学反应方程式中速率之比等于化学计量数之比,故A(g)+ 3B (g)
2NH3(g) △H=-93kJ·mol—1,往恒容密闭容器中充入0.4 molN2(g)和2 mol H2(g)达到平衡时,由于是可逆反应,因此放出的热量小于37.2 kJ ,故C错误;D. 根据化学反应方程式中速率之比等于化学计量数之比,故A(g)+ 3B (g) ![]() 2C (g) + D (g),在两种不同情况下的反应速率分别为:①vB=0.6mol/(L·min),②vC=0.4mol/(L·min),由于条件不同,因此两者速率无法比较,故D错误;答案:A。
2C (g) + D (g),在两种不同情况下的反应速率分别为:①vB=0.6mol/(L·min),②vC=0.4mol/(L·min),由于条件不同,因此两者速率无法比较,故D错误;答案:A。

【题目】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点。完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:CO2(g)+4H2(g)![]() CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
CH4(g)+2H2O(g),已知H2的体积分数随温度的升高而增加.若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化。(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
________ | ________ | ________ | ________ |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为________.
(3)碳酸:H2CO3 , K1=4.3×10﹣7 , K2=5.6×10﹣11 草酸:H2C2O4 , K1=5.9×10﹣2 , K2=6.4×10﹣5 ,0.1mol/LNa2CO3溶液的pH____0.1mol/LNa2C2O4溶液的pH,(选填“大于”“小于”或“等于”),等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是___.
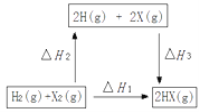
(4)在如图的转化关系中(X代表卤素)。ΔH2_____0(填“>”、“=”或“<”);△H1、△H2和△H3三者存在的关系为_______。
(5)现有浓度均为0.1mol·L-1的下列溶液:①硫酸、②醋酸、③氢氧化钠、④醋酸钠。请回答下列问题:
①醋酸钠中各离子浓度由大到小的顺序是_______。
②醋酸和醋酸钠等体积混合所得溶液中:c(CH3COOH)+c(CH3COO-)=______mol·L-1。
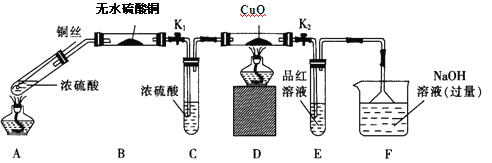
【题目】北京市场销售的某种食用精制盐包装袋上有如下说明:
产品标准 | GB5461 |
产品等级 | 一级 |
配 料 | 食盐、碘酸钾、抗结剂 |
碘含量(以I计) | 20~50mg/kg |
分装时期 | |
分装企业 |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
____KIO3+___KI+___H2SO4=___K2SO4+___I2+___H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是_________________________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及在上述步骤中的位置是______________________。
(3)已知:I2+2S2O32-=2I-+S4O62-。某学生测定食用精制盐的碘含量,其步骤为:
a. 准确称取wg食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,逐滴加入物质的量浓度为2.0×10-3mol·L-1的Na2S2O3溶液10.0mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是______________________。
②b中反应所产生的I2的物质的量是___________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)
_______________________mg/kg。