题目内容
【题目】已知:原子序数小于18的同一主族的两种元素X和Y,其原子半径:X<Y。下列说法正确的是
A. 若X和Y均位于VIIA,则键能大小为HX<HY
B. 若X和Y均位于VIA,则H2X分子间易形成氢键
C. 若X和Y均位于IVA,则二者最高价氧化物的晶体类型相同
D. 若X和Y均位于IIA,则第一电离能大小为X<Y
【答案】B
【解析】
A.若X和Y均位于VIIA,且原子半径:X<Y,所以X为F、Y为Cl,氢化物的稳定性HF![]() HCl,键能大小为HF
HCl,键能大小为HF![]() HCl,故A错误;
HCl,故A错误;
B.若X和Y均位于VIA,且原子半径:X<Y,所以X为O、Y为S,H2O分子间易形成氢键,故B正确;
C.若X和Y均位于IVA,且原子半径:X<Y,所以X为C、Y为Si,CO2是分子晶体,而SiO2是原子晶体,故C错误;
D.若X和Y均位于IIA, 且原子半径:X<Y,所以X为Be、Y为Mg, 第一电离能Be![]() Mg,故D错误;
Mg,故D错误;
本题答案为B。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
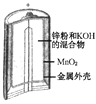
【题目】有关下列四个常用电化学装置的叙述中,正确的是( )
|
|
|
|
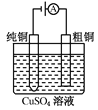
图Ⅰ 碱性锌锰电池 | 图Ⅱ铅硫酸蓄电池 | 图Ⅲ 电解精炼铜 | 图Ⅳ 银锌纽扣电池 |
A. 图Ⅰ所示电池中,MnO2的作用是催化剂
B. 图Ⅱ所示电池放电过程中,正极质量不断增大
C. 图Ⅲ所示装置工作过程中,电解质溶液浓度始终不变
D. 图Ⅳ所示电池中,放电时,负极附近溶液的pH不变