题目内容
Ⅰ.小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式: 。
Ⅱ.氨气通入水中可制得氨水,氨水能使无色的酚酞变红。请写出实验室制取氨气的化学方程式: ,
检验氨气的一种化学方法是: 。
Ⅲ.火药是中国的“四大发明”之一,黑火药在发生爆炸时,发生如下的反应:2KNO3+C+S=K2S+2NO2↑+CO2↑。其中氧化剂是 ;还原剂是 。
(1)HCO3- + H+ = CO2 ↑+ H2O (2)Ca(OH)2 + 2NH4Cl  CaCl2 + 2NH3↑+ 2H2O
CaCl2 + 2NH3↑+ 2H2O
用蘸有浓盐酸的玻璃棒靠近,产生白烟(或:用湿润的红色石蕊试纸靠近,变蓝色)
(3)KNO3和S, C
解析试题分析:Ⅰ 、胃液的主要成分为盐酸,小苏打与盐酸反应生成氯化钠、水和二氧化碳,离子方程式为HCO3- + H+ = CO2 ↑+ H2O;Ⅱ、实验室制取氨气可利用氯化铵和氢氧化钙在加热条件下反应生成氯化钙、氨气和水,化学方程式为Ca(OH)2 + 2NH4Cl  CaCl2 + 2NH3↑+ 2H2O;Ⅲ、反应:2KNO3+C+S=K2S+2NO2↑+CO2↑中,KNO3中氮元素的化合价由+5价降为+4价,硫单质中硫元素的化合价由0价降为—2价,所以氧化剂为KNO3和S,碳元素的化合价由0价升高到+4价,还原剂是C。
CaCl2 + 2NH3↑+ 2H2O;Ⅲ、反应:2KNO3+C+S=K2S+2NO2↑+CO2↑中,KNO3中氮元素的化合价由+5价降为+4价,硫单质中硫元素的化合价由0价降为—2价,所以氧化剂为KNO3和S,碳元素的化合价由0价升高到+4价,还原剂是C。
考点:考查氧化还原反应、离子方程式及化学方程式的书写。

 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案有一种白色粉末,含有下列阴离子和阳离子中的几种。
阴离子:S2-、Cl-、NO3—、SO42—、CO32—、HCO3—、MnO4—。
阳离子:Na+、Mg2+、Al3+、Ba2+、Fe2+、Fe3+、Cu2+、NH4+。
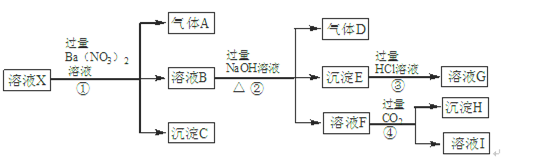
将该白色粉末进行下列实验,观察到的现象如下:
| 实验操作 | 现象 |
| a.取少量粉末,加水、振荡 | 全部溶解、 |
| 溶液无色透明 | |
| b.向所得溶液中慢慢滴入苛性钠溶液,并加热 | 无明显现象 |
| c.取少量粉末,加盐酸 | 无明显现象 |
| d.取少量粉末,加稀H2SO4和稀HNO3的混合液 | 有白色沉淀生成 |
根据实验推断:
(1)从a实验中,可推断粉末中不可能有______________(填离子符号,下同)。
(2)从b实验中,可推断粉末中不可能有_____________________________________。
(3)从c实验中,可推断粉末中不可能有________________________________。
(4)从d实验中,可推断粉末中不可能有________,一定含有________。
(5)以上各实验仍无法确定是否存在的离子是____________。
1 L 某混合溶液,可能含有的离子如下表:
| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、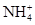 、Fe2+、Fe3+ 、Fe2+、Fe3+ |
| 可能大量含有的阴离子 | Cl-、Br-、I-、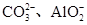 |
(1)往该溶液中逐滴加入NaOH溶液,产生沉淀的物质的量(n)与加入NaOH溶液的体积(V)的关系如图所示。则该溶液中一定不含有的离子是________________。

(2)BC段的离子方程式为__________________________。
(3)V1、V2与V3、V4之间的关系为____________________。
(4)经检测,该溶液中还含有大量的Cl-、Br-、I-,若向1 L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br-、I-的物质的量与通入Cl2的体积(标准状况)的关系如表所示,分析后回答下列问题:
| Cl2的体积(标准状况) | 2.8 L | 5.6 L | 11.2L |
| n(Cl-) | 1.25 mol | 1.5 mol | 2 mol |
| n(Br-) | 1.5 mol | 1.4 mol | 0.9 mol |
| n(I-) | a mol | 0 | 0 |
①当通入Cl2的体积为2.8 L时,溶液中发生反应的离子方程式为____________________。
②原溶液中Cl-、Br-、I-的物质的量浓度之比为_________________。
 CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题:
CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电。下图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝。回答下列问题: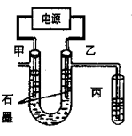
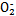 可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。
可用铝粉除去。已知此反应体系中含有Al、NaAlO2、NaNO2、NaOH、NH3·H2O、H2O六种物质。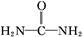 )与N
)与N