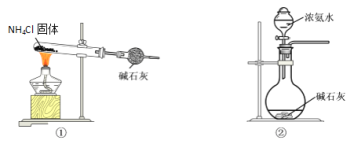
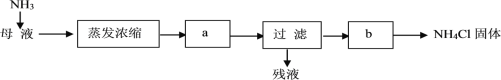
题目内容
【题目】![]() 是一种饲料营养强化剂。一种利用水钴矿(主要成分为
是一种饲料营养强化剂。一种利用水钴矿(主要成分为![]() 、
、![]() ,还含少量
,还含少量![]() 、
、![]() 、MnO等),制取
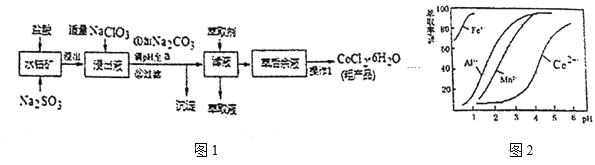
、MnO等),制取![]() 的工艺流程如图1:
的工艺流程如图1:
已知:①浸出液含有的阳离子主要有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等;
等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:(金属离子浓度为:0.01mol/L)
③![]() 熔点为86℃,加热至110~120℃时,失去结晶水生成无水氧化钴。
熔点为86℃,加热至110~120℃时,失去结晶水生成无水氧化钴。
沉淀物 |
|
|
|
|
|
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中![]() 发生反应的离子方程式____。
发生反应的离子方程式____。
(2)写出NaClO3发生反应的主要离子方程式____,若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式____。
(3)“加![]() 调pH至a”,过滤所得到的沉淀成分为___。
调pH至a”,过滤所得到的沉淀成分为___。
(4)制得的![]() 在烘干时需减压烘干的源因是___。
在烘干时需减压烘干的源因是___。
(5)萃取剂对金属高子的萃取率与pH的关系如图2。向“滤液”中加入萃取剂的目的是___﹔其使用的最佳pH范围是___。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
【答案】![]()
![]()
![]()
![]() 、
、![]() 降低烘干温度,防止产品分解 除去溶液中的
降低烘干温度,防止产品分解 除去溶液中的![]() B
B
【解析】
含钴废料中加入盐酸和亚硫酸钠,可得CoCl2、AlCl3、FeCl2,加入NaClO3,可得到FeCl3,然后加入Na2CO3调pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,过滤后所得滤液主要含有CoCl2,为得到CoCl26H2O晶体,应控制温度在86℃以下,加热时要防止温度过高而失去结晶水,可减压烘干。
(1)向水钴矿主要成分为![]() 、
、![]() ,还含少量
,还含少量![]() 、
、![]() 、MnO等,加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有
、MnO等,加入盐酸和亚硫酸钠,浸出液含有的阳离子主要有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等,所以
等,所以![]() 和亚硫酸钠在酸性条件下发生氧化还原,根据电荷守恒和得失电子守恒,反应的离子方程式为:
和亚硫酸钠在酸性条件下发生氧化还原,根据电荷守恒和得失电子守恒,反应的离子方程式为: ![]() ,
,
(2)![]() 的作用是将
的作用是将![]() 氧化成
氧化成![]() ,其反应的离子方程式为:
,其反应的离子方程式为:![]() ;在酸性条件下,
;在酸性条件下, ![]() 与氯离子发生氧化还原反应生成氯气,其反应的离子方程式为:
与氯离子发生氧化还原反应生成氯气,其反应的离子方程式为:![]() ↑
↑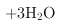 ;
;
(3) ![]() 的作用是将
的作用是将![]() 氧化成
氧化成![]() ,加
,加![]() 调pH至a,铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:
调pH至a,铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:![]() ↓
↓![]() ↑;铁离子能与碳酸根离子发生双水解生成氢氧化铁和二氧化碳,水解的离子方程式为:
↑;铁离子能与碳酸根离子发生双水解生成氢氧化铁和二氧化碳,水解的离子方程式为:![]() ↓
↓![]() ↑,所以沉淀成分为:
↑,所以沉淀成分为:![]() 、
、![]() ,
,
(4)利用从溶液中制取固体的方法制取氯化钴固体,其操作步骤为:蒸发浓缩、冷却结晶和过滤,
(5)根据流程图可以知道,此时溶液中存在![]() 、
、![]() 金属离子; 由萃取剂对金属离子的萃取率与pH的关系可以知道,调节溶液pH在3.0~3.5之间,可使
金属离子; 由萃取剂对金属离子的萃取率与pH的关系可以知道,调节溶液pH在3.0~3.5之间,可使![]() 完全沉淀,并防止
完全沉淀,并防止![]() 转化为
转化为![]() 沉淀。
沉淀。

 超能学典应用题题卡系列答案
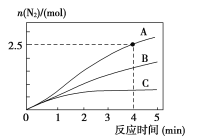
超能学典应用题题卡系列答案【题目】某反应在体积为5L的恒容密闭的绝热容器中进行,各物质的量随时间的变化情况如下图所示(已知A、B、C均为气体)。

(1)该反应的化学方程式为_______。
(2)反应开始至2分钟时,B的平均反应速率为_______。
(3)能说明该反应已达到平衡状态的是_______
A.υ(A)=2υ(B) B.容器内气体密度不变
C.v逆(A)=υ正(C) D.各组分的物质的量相等
E. 混合气体的平均相对分子质量不再改变的状态
(4)由图求得平衡时A的转化率为_______。
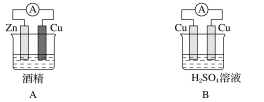
(5)为了研究硫酸铜的量对氢气生成速率的影响,某同学设计了如下一系列的实验:将表中所给的混合溶液分别加入到6个盛有过量Zn粒的容器中,收集产生的气体,记录获得相同体积的气体所需时间。
实验 混合溶液 | A | B | C | D | E | F |
4 mol/L H2SO4(mL) | 30 | V1 | V2 | V3 | V4 | V5 |
饱和CuSO4溶液(mL) | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
H2O(mL) | V7 | V8 | V9 | V10 | 10 | 0 |
①请完成此实验设计,其中:V1=_______,V6=_______。
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因_______。