题目内容
【题目】1942年,我国化工专家侯德榜以NaCl、NH3、CO2等为原料制得纯碱,他的“侯氏制碱法”为世界制碱工业做出了突出贡献。回答下列问题:
某探究活动小组欲在实验室中模拟制取纯碱,设计了Ⅰ、Ⅱ两种方案,并选择其一进行实验。
方案Ⅰ:(1)将足量CO2通入饱和NaCl溶液中;(2)再在所得溶液中通入足量NH3;(3)过滤;
方案Ⅱ:(1)将足量NH3通入饱和NaCl溶液中;(2)再在所得溶液中通入足量CO2;(3)过滤;
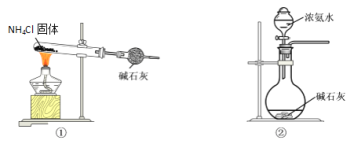
(1)部分实验装置如图所示。制取氨气的装置应选用________(选填编号)。
(2)写出实验中获得碳酸氢钠的离子方程式____________
(3)灼烧碳酸氢钠需要_________(选填编号)。
a.蒸发皿 b.坩埚 c.烧杯 d.烧瓶 e.酒精灯
(4)选择的实验方案是________(选填“Ⅰ”或“Ⅱ”),说明选择的理由_____________
(5)甲同学取少量产品完全溶于水,滴加稀硝酸2-3滴,再滴加硝酸银溶液,观察到有白色沉淀生成,得出纯碱含杂质Cl-的结论。乙同学认为甲的结论不一定正确,你认为乙同学的理由是____。
(6)按下列流程处理母液(提取完碳酸氢钠后的滤液)可得到NH4Cl。
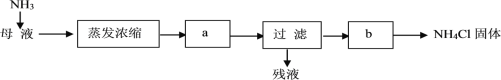
通入NH3的作用是_______(选填编号)。
a.增大NH4+浓度,使NaHCO3更多地析出
b.增大NH4+浓度,使NH4Cl更多地析出
c.使NaHCO3转化为溶解度更大的Na2CO3,提高析出的NH4Cl纯度
【答案】② CO2+H2O+NH3+Na+→NaHCO3↓+NH4+ b、e Ⅱ 因二氧化碳气体溶解度较小,若先通入二氧化碳气体再通入氨气后,生成的碳酸氢钠量较少,难以析出沉淀 稀硝酸可能不足,没有把碳酸钠完全反应掉 bc
【解析】
(1)实验室制备氨气的方法是利用氯化铵和氢氧化钙加热反应生成或利用浓氨水滴入固体氢氧化钠或氧化钙或碱石灰中生成氨气;
(2)氨化的饱和氯化钠溶液中通入二氧化碳生成碳酸氢钠晶体和氯化铵;
(3)灼烧固体在坩埚中进行;
(4)氨气极易溶于水,二氧化碳能溶于水,所以应先通入氨气,从而保证了通入二氧化碳时,二氧化碳被充分反应;
(5)碳酸钠和硝酸银反应也能生成碳酸银白色沉淀;
(6)通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度,蒸发浓缩、冷却结晶、过滤洗涤、干燥等操作得到晶体。
(1)装置①加热分解氯化铵生成氨气和氯化氢在试管口处重新生成氯化铵,不能制得大量氨气,②装置浓氨水滴入碱石灰固体溶解过程中放热,一水合氨分解生成氨气,可以制备氨气,故答案为②;
(2)氨化的饱和氯化钠溶液中通入二氧化碳生成碳酸氢钠晶体和氯化铵,反应的离子方程式:CO2+H2O+NH3+Na+=NaHCO3↓+NH4+;
(3)灼烧碳酸氢钠需要在坩埚中加热灼烧,选择be,故答案为:b、e;
(4)将足量NH3通入饱和NaCl溶液中,再在所得溶液中通入足量CO2,氨气极易溶于水,二氧化碳能溶于水,所以应先通入氨气,从而保证了通入二氧化碳时,二氧化碳被充分反应,因二氧化碳气体溶解度较小,若先通入二氧化碳气体再通入氨气后,生成的碳酸氢钠量较少,难以析出沉淀;
(5)甲同学取少量产品完全溶于水,滴加稀硝酸2-3滴,再滴加硝酸银溶液,观察到有白色沉淀生成,得出纯碱含杂质Cl-的结论,乙同学认为甲的结论不一定正确,理由是:稀硝酸可能不足,没有把碳酸钠完全反应掉;
(6)根据NH3+H2O+CO2+NaCl═NH4Cl+NaHCO3↓及流程图知,母液中溶质为氯化铵,向母液中通氨气加入细小食盐颗粒,冷却析出副产品,通入的氨气和水反应生成一水合氨,一水合氨电离出铵根离子,铵根离子浓度增大有利于析出氯化铵,通入氨气使溶液碱性增强,使碳酸氢钠转换为溶解度较大的碳酸钠,可以提高氯化铵的纯度所故bc正确,故答案为:bc。

 举一反三同步巧讲精练系列答案
举一反三同步巧讲精练系列答案 口算与应用题卡系列答案
口算与应用题卡系列答案【题目】![]() 是一种饲料营养强化剂。一种利用水钴矿(主要成分为
是一种饲料营养强化剂。一种利用水钴矿(主要成分为![]() 、
、![]() ,还含少量
,还含少量![]() 、
、![]() 、MnO等),制取
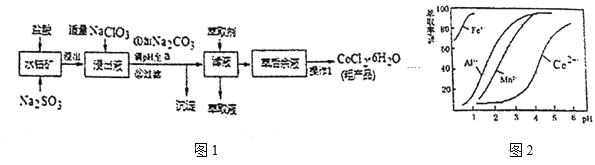
、MnO等),制取![]() 的工艺流程如图1:
的工艺流程如图1:
已知:①浸出液含有的阳离子主要有![]() 、
、![]() 、
、![]() 、
、![]() 、
、![]() 等;
等;
②部分阳离子以氢氧化物形式沉淀时溶液的pH见表:(金属离子浓度为:0.01mol/L)
③![]() 熔点为86℃,加热至110~120℃时,失去结晶水生成无水氧化钴。
熔点为86℃,加热至110~120℃时,失去结晶水生成无水氧化钴。
沉淀物 |
|
|
|
|
|
开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
(1)写出浸出过程中![]() 发生反应的离子方程式____。
发生反应的离子方程式____。
(2)写出NaClO3发生反应的主要离子方程式____,若不慎向“浸出液”中加过量NaClO3时,可能会生成有毒气体,写出生成该有毒气体的离子方程式____。
(3)“加![]() 调pH至a”,过滤所得到的沉淀成分为___。
调pH至a”,过滤所得到的沉淀成分为___。
(4)制得的![]() 在烘干时需减压烘干的源因是___。
在烘干时需减压烘干的源因是___。
(5)萃取剂对金属高子的萃取率与pH的关系如图2。向“滤液”中加入萃取剂的目的是___﹔其使用的最佳pH范围是___。
A.2.0~2.5 B.3.0~3.5 C.4.0~4.5 D.5.0~5.5
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
|
|
|
① | ② | ③ |
A. 由①中的红棕色气体,推断产生的气体一定是混合气体
B. 红棕色气体不能表明②中木炭与浓硝酸产生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应