题目内容
12.有A、B、C、D四种金属,投入水中只有D反应放出氢气,将A投入C的盐溶液中可置换出金属C,B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,则四种金属的金属性强弱顺序正确的是( )| A. | A>B>C>D | B. | A>C>B>D | C. | A>C>D>B | D. | D>B>A>C |
分析 金属的金属性越强,其单质与酸或水反应生成氢气越容易,其最高价氧化物的水化物碱性越强;较活泼的金属能置换出较不活泼金属,据此判断金属性强弱.
解答 解:金属的金属性越强,其单质与酸或水反应生成氢气越容易,其最高价氧化物的水化物碱性越强;较活泼的金属能置换出较不活泼金属,只有D能与水反应生成氢气,说明D金属性很强;
将A投入C的盐溶液中可置换出金属C,说明金属性A>C;
B的最高价氧化物的水化物碱性比A的最高价氧化物的水化物碱性强,说明金属性B>A,
所以金属性强弱顺序是D>B>A>C,故选D.
点评 本题考查金属的金属性强弱判断,金属的金属性强弱判断方法有:金属与酸或水反应生成氢气难易程度、其最高价氧化物的水化物碱性强弱、金属之间的置换反应等,注意不能根据失电子多少判断金属性强弱,要根据失电子难易程度判断金属性强弱.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
2.一定量的Cu粉与浓H2SO4共热产生SO2气体的体积为2.24L(标准状况下),则下列情况不可能的是( )
| A. | 加入Cu的质量为6.4g | B. | 加入Cu的质量大于6.4g | ||
| C. | 加入浓H2SO4中含溶质为0.2mol | D. | 加入浓H2SO4中含溶质大于0.2mol |
3.下列说法正确的是( )
| A. | 同周期ⅠA族元素的金属性比ⅡA族元素的金属性强 | |
| B. | 同一周期元素的原子,半径越小越容易失去电子 | |
| C. | 同周期非金属氧化物对应的水化物的酸性从左到右依次增强 | |
| D. | 第3周期元素的离子半径从左到右逐渐减小 |
20.要想除去丙烷中的乙烯并得到纯净的丙烷,可选择的试剂是( )
| A. | NaOH 溶液、浓H2SO4 | B. | 溴的四氯化碳溶液、浓H2SO4 | ||
| C. | 乙醇、浓H2SO4 | D. | 酸性高锰酸钾溶液、浓H2SO4 |
17.下列除杂质的方案不可行的是( )
| A. | 用饱和碳酸钠溶液除去乙酸乙醋中的乙酸和乙醇 | |
| B. | 用加人NaOH 溶液、分液的方法来分离甲苯和苯酚的混合液 | |
| C. | 用渗析的方法对蛋白质胶体进行提纯,以净化蛋白质胶体 | |
| D. | 用酸性高锰酸钾溶液除去乙烷中的乙烯 |
15.丙烷是一种重要的烷烃,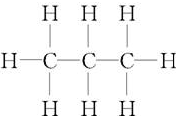 表示其( )
表示其( )
 表示其( )
表示其( )| A. | 结构简式 | B. | 结构式 | C. | 电子式 | D. | 分子式 |
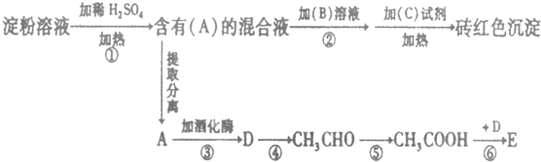
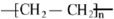 .
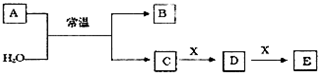
.
 ;
;