题目内容
9.有德国重离子研究中心人工合成的第112号元素的正式名称为“Copernicium”,相应的元素符号位“Cn”.该元素的名称是为了纪念天文学家哥白尼而得名.该中心人工合成Cn的过程可表示为:7030Zn+20882Pb═277112Cn+10n.下列叙述中正确的是( )| A. | 277112Cn的原子核内中子数比质子数多53 | |
| B. | Cn元素的相对原子质量为277 | |
| C. | 上述合成过程中属于化学变化 | |
| D. | Cn元素位于元素周期表的第六周期,是副族元素 |
分析 A.该原子的中子数=质量数-质子数,据此计算出中子数与质子数之差;
B.元素的相对原子量与原子的相对原子量和在自然界中的含量有关,277只表示该原子的相对原子质量;
C.化学变化的最小微粒为原子,该反应前后原子的类型发生了变化;
D.第118编号元素位于周期表中第七周期、零族,据此判断112号元素在周期表中的位置.
解答 解:A.该原子的中子数=277-112,质子数比质子数多的数目为:277-112-112=53,故A正确;
B.该Cn原子的相对原子质量为277,元素的相对原子量与原子的相对原子量和在自然界中的含量有关,故B错误;
C.化学变化的最小粒子为原子,该反应中原子类型发生了变化,不属于化学变化,故C错误;
D.第118编号元素位于周期表中第七周期、零族,则112号元素位于第七周期、ⅡB族,故D错误;
故选A.
点评 本题考查了原子结构、元素的相对原子量与原子的相对原子量之间的关系,题目难度不大,注意掌握原子中质量数与质子数、中子数之间的关系,明确元素的相对原子量与原子的相对原子量的关系.

练习册系列答案
相关题目
5.下列各组离子一定能大量共存的是( )
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在使酚酞变红的溶液中:Na+、K+、AlO2-、CO32- | |
| C. | 在水电离产生的c(OH-)=1×10-14mol•L-1的溶液中:NH4+、Al3+、SO42-、NO3- | |
| D. | 在pH试纸变深红色的溶液中:K+、Fe2+、Cl-、NO3- |
3.根据下列实验事实判断所测液体样品最有可能是纯水的是( )
| A. | 室温下测定其pH等于7 | |
| B. | 一个标准大气压下测定其沸点为100℃ | |
| C. | 电解时产生H2、O2的体积比为2:1 | |
| D. | 室温时为无色的液体 |
4.下列说法不正确的是( )
| A. | 原子半径Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 碱性:KOH>NaOH>Mg(OH)2 | D. | 酸性强弱:H2SiO3<H2CO3<H3PO4 |
14.下列物质加入水中,显著放热的是( )
| A. | 生石灰 | B. | 固体NaOH | C. | 无水乙醇 | D. | 固体硝酸铵 |
1. (1)下列数据是对应物质的熔点(℃)
(1)下列数据是对应物质的熔点(℃)
据此作出的下列判断中,错误的是AB
A、铝的化合物晶体中不存在离子晶体
B、表中只有BCl3、干冰是分子晶体
C、同族元素的氧化物可形成不同类型的晶体
D、不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图( )所示.SiO2晶体中Si原子数目和Si-O键数目的比例为1:4.
)所示.SiO2晶体中Si原子数目和Si-O键数目的比例为1:4.
通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.
Si(s)+O2(g)$\frac{\underline{\;高温\;}}{\;}$ SiO2(s),该反应的反应热△H=-990 kJ/mol
(3)与铝同周期的磷单质及其化合物有广泛应用.
①三聚磷酸可视为三个磷酸分子(磷酸结构式见图 )之间脱去两个水分子产物,其结构式为
)之间脱去两个水分子产物,其结构式为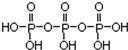 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
②次磷酸钠(NaH2PO2)可用于化学镀镍.NaH2PO2中P元素的化合价为+1;
化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)1 Ni2++1 H2PO2-+1H2O→1 Ni+1 H2PO3-+2H+
(b)6H2PO2-+2H+=2P+4H2PO3+3H2
(4)氢气是新型清洁能源,镧(La)和镍的合金可做储氢材料.该合金的晶胞如图所示,晶胞中心有一镍原子,其它镍原子都在晶胞面上,该晶体的化学式是Ni5La.
 (1)下列数据是对应物质的熔点(℃)
(1)下列数据是对应物质的熔点(℃)| NaCl | Na2O | AlF3 | AlCl3 | BCl3 | Al2O3 | CO2 | SiO2 |
| 801 | 920 | 1291 | 190 | -109 | 2073 | -57 | 1723 |
A、铝的化合物晶体中不存在离子晶体
B、表中只有BCl3、干冰是分子晶体
C、同族元素的氧化物可形成不同类型的晶体
D、不同族元素的氧化物可形成不同类型的晶体
(2)SiO2晶体结构片断如图(
 )所示.SiO2晶体中Si原子数目和Si-O键数目的比例为1:4.
)所示.SiO2晶体中Si原子数目和Si-O键数目的比例为1:4.通常人们把拆开1mol 某化学键所吸收的能量看成该化学键的键能.
| 化学键 | Si-O | Si-Si | O=O |
| 键能/KJ•mol-1 | 460 | 176 | 498 |
(3)与铝同周期的磷单质及其化合物有广泛应用.
①三聚磷酸可视为三个磷酸分子(磷酸结构式见图
 )之间脱去两个水分子产物,其结构式为
)之间脱去两个水分子产物,其结构式为 .三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.
.三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为Na5P3O10.②次磷酸钠(NaH2PO2)可用于化学镀镍.NaH2PO2中P元素的化合价为+1;
化学镀镍的溶液中含有Ni2+和H2PO2-,在酸性等条件下发生下述反应:
(a)1 Ni2++1 H2PO2-+1H2O→1 Ni+1 H2PO3-+2H+
(b)6H2PO2-+2H+=2P+4H2PO3+3H2
(4)氢气是新型清洁能源,镧(La)和镍的合金可做储氢材料.该合金的晶胞如图所示,晶胞中心有一镍原子,其它镍原子都在晶胞面上,该晶体的化学式是Ni5La.
18.著名化学家徐光宪获得国家最高科学技术奖,以表彰他在稀土萃取理论方面作出的贡献.已知:金属铈(稀土元素)在空气中易氧化变暗,受热时燃烧,遇水很快反应.(注:铈常见的化合价为+3和+4,氧化性:Ce4+>Fe3+>I2.)下列说法正确的是( )
| A. | 铈溶于氢碘酸的化学方程式可表示为:Ce+4HI $\frac{\underline{\;高温\;}}{\;}$ CeI4+2H2↑ | |
| B. | 用Ce(SO4)2溶液滴定硫酸亚铁溶液,其离子方程式为:Ce4++2Fe2+═Ce3++2Fe3+ | |
| C. | 金属Ce保存时,应该隔绝空气和水 | |
| D. | 铈的四种核素136 58Ce、138 58Ce、140 58Ce、142 58Ce,它们互称为同素异形体 |
19.下面有关叙述正确的是( )
| A. | 13C与15N有相同的中子数 | |
| B. | 1H2O与2H2O互为同素异形体 | |
| C. | 14C与14N互为同位素 | |
| D. | CH3-CH2OH和CH3-O-CH3互为同分异构体 |