题目内容
【题目】I.常温下,将某一元酸HA和NaOH溶液等体积混合,分别进行编号为①、②、③的实验,实验数据记录如下表。
序号 | HA物质的量浓度(molL-1) | NaOH物质的量浓度(molL-1) | 混合溶液的pH |
① | 0.1 | 0.1 | pH=9 |
② | c | 0.2 | pH=7 |
③ | 0.2 | 0.1 | pH<7 |
(1)根据①组实验情况,分析混合溶液的pH=9的原因是______________________(用离子方程式表示),在该溶液中下列关系式错误的是________________(填标号)。
a.c(Na+)+c(H+)=c(OH-)+c(A-) b.c(Na+)=c(HA)+c(A-)
c.c(HA)+c(H+)=c(OH-) d.c(Na+)+c(H+)=c(OH-)+c(A-)+c(HA)
(2)②组情况表明,c______0.2(填“>”“<”或“=”,下同),混合溶液中:c(A-)_______c(Na+)。
(3)从③组实验结果分析,说明HA的电离程度_____NaA的水解程度(填“>”“<”或“=”),离子浓度由大到小的顺序是_______________________________。
Ⅱ.室温下,若将0.1 molL-1盐酸滴入20mL0.1 molL-1氨水中,溶液pH随加入盐酸体积的变化曲线如下图所示:
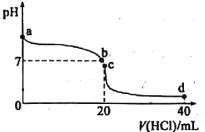
(1)NH3·H2O的电离方程式是_______________________________。
(2)b点所示溶液中的溶质是_______________________________。
(3)c点所示溶液中,离子浓度从大到小的关系为_______________________________。
【答案】 A-+H2O![]() HA+OH- d > = > c(A-)>c(Na+)>c(H+)>c(OH-) NH3·H2O
HA+OH- d > = > c(A-)>c(Na+)>c(H+)>c(OH-) NH3·H2O![]() NH4++OH- NH4Cl 和NH3·H2O c(Cl-)>c(NH4+)>c(H+)>c(OH-)
NH4++OH- NH4Cl 和NH3·H2O c(Cl-)>c(NH4+)>c(H+)>c(OH-)
【解析】试题分析:Ⅰ、(1)HA与NaOH等体积、等浓度混合,恰好反应生成NaA,若NaA是强碱弱酸盐,A-水解溶液显碱性,所以PH>9,则混合溶液的pH=9的原因是A-+H2O![]() HA-+OH-;A.根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(A-),正确;B.根据物料守恒,c(Na+)=c(HA)+c(A-)正确;C.根据质子守恒c(HA)+c(H+)=c(OH-),正确;选D。
HA-+OH-;A.根据电荷守恒c(Na+)+c(H+)=c(OH-)+c(A-),正确;B.根据物料守恒,c(Na+)=c(HA)+c(A-)正确;C.根据质子守恒c(HA)+c(H+)=c(OH-),正确;选D。
(2)NaA溶液呈碱性,要使混合溶液呈中性,则HA应该稍微过量,二者体积相等,所以c>0.2molL-1,根据电荷守恒,c(Na+)+c(H+)=c(OH-)+c(A-),c(H+)=c(OH-),则c(A-)=(Na+)。
(3)从③组实验结果可以看出,等物质的量浓度的NaA和HA溶液呈酸性,说明酸的电离程度大于酸根离子水解程度,溶液呈酸性,则c(H+)>c(OH-),根据电荷守恒得c(A-)>c(Na+),溶液中酸的电离较微弱,所以c(Na+)>c(H+),则溶液中离子浓度大小顺序是c(A-)>c(Na+)>c(H+)>c(OH-)。
Ⅱ、(1)NH3·H2O是弱碱,电离方程式是NH3·H2O![]() NH
NH![]() +OH–,
+OH–,
(2)等浓度等体积的氨水和HCl恰好反应,生成NH4Cl ,NH4Cl 属于强酸弱碱盐,水解显酸性。要想使溶液显中性,氨水需多加点,则b点所示溶液中的溶质是NH4Cl和NH3·H2O;
(3)c点所示的溶液是等浓度等体积的氨水和HCl恰好反应,生成的氯化铵水解显酸性,离子浓度从大到小的关系为c (Cl–) >c (NH4+)>c (H+)>c (OH–)。

 名校课堂系列答案
名校课堂系列答案