题目内容
17.已知H2(g)+Br2(g)═2HBr(g)△H=-70KJ/mol,其它相关数据如下表:| H2(g) | Br2(g) | HBr(g) | |
| 1mol 分子中的化学键断裂时需要吸收的能量/KJ | 410 | a | 370 |
| A. | 400 | B. | 260 | C. | 230 | D. | 200 |
分析 1molH2(g)化学键断裂时需要吸收的能量为410kJ,1molBr2(g)化学键断裂时需要吸收的能量为akJ,1molHBr(g)化学键断裂时需要吸收的能量为370kJ,依据△H=反应物的总键能-生成物的总键能列方程计算.
解答 解:1molH2(g)化学键断裂时需要吸收的能量为410kJ,1molBr2(g)化学键断裂时需要吸收的能量为akJ,1molHBr(g)化学键断裂时需要吸收的能量为370kJ,H2(g)+Br2(g)═2HBr(g)△H=-70kJ•mol-1,依据△H=反应物的总键能-生成物的总键能,则-70=410+a-370×2,a=260,
故选B.
点评 本题考查反应热的计算,题目难度不大,注意反应热与键能的计算关系,明确△H=反应物的总键能-生成物的总键能是解题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.用赤铁矿为原料冶炼铁,应采取的冶炼方法是( )
| A. | 电解法 | B. | 热氧化法 | C. | 热还原法 | D. | 热分解法 |
8.下列说法中正确的是( )
| A. | 硫酸的摩尔质量是98 g | |
| B. | 摩尔是物质质量的单位 | |
| C. | 氮原子的质量就是氮的相对原子质量 | |
| D. | 氧气的摩尔质量(单位:g•mol-1)在数值上等于它的相对分子质量 |
5.下列化学反应中,硝酸既表现了氧化性又表现了酸性的是( )
| A. | 氧化铁与硝酸反应 | B. | 木炭与浓硝酸反应 | ||
| C. | 铜与硝酸反应 | D. | 氢氧化铝与硝酸反应 |
12.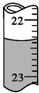 用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( )
用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( )
 用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( )
用0.102 6mol•L-1的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为( )| A. | 22.30 mL | B. | 22.35 mL | C. | 23.65 mL | D. | 23.70 mL |
9.下列图示与对应的叙述相符的是( )


| A. | 图1表示相同温度下pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 | |
| B. | 图2中纯水仅升高温度,就可以从a点变到c点 | |
| C. | 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 | |
| D. | 用0.0100mol/L硝酸银标准溶液,滴定Cl-、Br-及I-且浓度均为0.1000mol/L的混合溶液,由图3曲线,可确定首先沉淀的是Cl- |
6.0.5 mol Na2CO3中所含的Na+数约为( )
| A. | 3.01×1023 | B. | 6.02×1023 | C. | 0.5 | D. | 1 |
 周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题:
周期表前四周期的元素a、b、c、d、e,原子序数依次增大.A的核外电子总数与其电子层数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍,d与c同主族,e的最外层只有1个电子,但次外层有18个电子.回答下列问题: .
.