题目内容
4.如图,实验室用如图所示装置制备溴苯,并验证该反应是取代反应.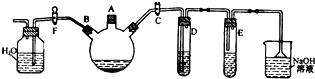
(1)关闭F活塞,打开C活塞,在装有少量苯的三颈烧瓶中由A口加入少量液溴,再加入少量铁屑,塞住A口,反应进行.
(2)D试管内装的是CCl4,其作用是除去挥发出来的溴.
(3)E试管内装的是硝酸银溶液,E试管内出现的现象为液面上方有白雾,溶液里有淡黄色沉淀生成.
(4)待三颈烧瓶中的反应即将结束时(此时气体明显减少),打开F活塞,关闭C活塞,可以看到的现象是水倒流进三口烧瓶.
(5)液溴滴完后,经过下列步骤分离提纯:
①向A中加入10mL水,然后过滤除去未反应的铁屑;
②滤液依次用10mL水、8mL10%的NaOH溶液、10mL水洗涤.
其中加入氢氧化钠反应化学方程式是:Br2+2NaOH=NaBr+NaBrO+H2O、HBr+NaOH=NaBr+H2O
③向分出的粗溴苯中加入少量的无水氯化钙,静置、过滤.加入氯化钙的目的是干燥;
(6)经以上分离操作后,粗溴苯中还含有的主要杂质为苯,要进一步提纯,下列操作中必须的是C(填入正确选项前的字母);
A.重结晶 B.过滤 C.蒸馏 D.萃取.
分析 实验室制备溴苯是用苯和液溴在铁粉作催化剂的条件下发生取代反应生成溴苯和溴化氢,根据装置图可知,生成溴苯的同进还有溴化氢生成另外还有少部分溴挥发,所以在D装置中石蕊会变红,E中的硝酸银会产生溴化银沉淀,尾气用氢氧化钠溶液吸收,关闭C打开F时,由于溴化氢极易溶于水,广口瓶中的水会倒吸入三颈烧瓶,
(2)由于反应放热,苯和液溴均易挥发,溴的存在干扰检验H+和Br-;
(3)E试管是用来检验HBr的,可结合溴化氢极易溶解于水,以及溴化氢和硝酸银反应的淡黄色沉淀是溴化银来分析实验现象;
(4)溴化氢极易溶于水,容易发生倒吸;
(5)②三口烧瓶中的溴苯含有少量的溴和溴化氢,可以用NaOH溶液除去;
③向分出的粗溴苯中加入少量的无水氯化钙,可以除去溴苯中少量的水;
(6)苯易溶在溴苯中,且和氢氧化钠溶液不反应,所以粗溴苯中还含有的主要杂质为苯,除去苯可以用蒸馏的方法.
解答 解:实验室制备溴苯是用苯和液溴在铁粉作催化剂的条件下发生取代反应生成溴苯和溴化氢,根据装置图可知,生成溴苯的同进还有溴化氢生成另外还有少部分溴挥发,所以在D装置中石蕊会变红,E中的硝酸银会产生溴化银沉淀,尾气用氢氧化钠溶液吸收,关闭C打开F时,由于溴化氢极易溶于水,广口瓶中的水会倒吸入三颈烧瓶,
(2)(1)由于反应放热,苯和液溴均易挥发,苯和溴极易溶于四氯化碳,用四氯化碳(CCl4)除去溴化氢气体中的溴蒸气和苯,以防干扰检验H+和Br-,
故答案为:CCl4;除去挥发出来的溴;
(3)E试管内装的试剂的作用为检验生成的溴化氢,因溴化氢易溶于水,液面上方会看到白雾,同时溶解于水的溴化氢电离出的溴离子和银离子反应,AgNO3+HBr=AgBr↓,生成淡黄色不溶于硝酸的沉淀溴化银,故答案为:硝酸银溶液;液面上方有白雾,溶液里有淡黄色沉淀生成;
(4)由于溴化氢极易溶于水,所以待三颈烧瓶中的反应进行到仍有气泡冒出时松开F夹,关闭C夹,可以看到的现象是与F相连的广口瓶中水流入三颈烧瓶,
故答案为:水倒流进三口烧瓶;
(5)②由于溴苯中溶有溴化氢与单质溴,所以氢氧化钠溶液的作用是吸收HBr和Br2,发生反应的化学方程式为Br2+2NaOH=NaBr+NaBrO+H2O、HBr+NaOH=NaBr+H2O,故答案为:Br2+2NaOH=NaBr+NaBrO+H2O、HBr+NaOH=NaBr+H2O;
③氯化钙是常用的干燥剂,起干燥作用,故答案为:干燥;
(6)苯易溶在溴苯中,且和氢氧化钠溶液不反应,所以粗溴苯中还含有的主要杂质为苯,二者的沸点相差较大,蒸馏即可分离,故选C,故答案为:苯;C.
点评 该题是高考中的常见题型,属于中等难度的试题,试题综合性强,难易适中.在注重对学生基础性知识考查和训练的同时,侧重对学生能力的培养和解题方法的指导与训练,有利于培养学生的严谨规范的实验设计能力,也有利于提高学生的学科素养.

| A. | 纳米铜能在氧气中燃烧,说明了纳米铜比普通铜的还原性强 | |
| B. | 白色污染与塑料垃圾有关 | |
| C. | 臭氧空洞的形成与化石燃料大量使用有关 | |
| D. | “海水淡化”可以解决“淡水供应危机”,向海水中加入净水剂明矾可以使海水淡化 |
| A. | 淀粉和纤维素的化学式都是(C6H10O5)n,故互为同分异构体 | |
| B. | 不含杂质的天然油脂属于高分子化合物,有固定的熔、沸点 | |
| C. | 蔗糖、植物油、天然蛋白质完全燃烧后的最终产物均为C02和H20 | |
| D. | 纤维素乙酸酯、油脂、蛋白质和麦芽糖在一定条件下都能水解 |
 目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:
目前工业上有一种方法是用CO2生产燃料甲醇.一定条件下发生反应:CO2+3H2?CH3OH+H2O,该反应的能量变化如图所示:(1)甲同学认为该反应为放热反应,他的理由为:反应物的总能大于生成物的总能量
(2)在体积为2L的密闭容器中,充入1mol CO2和3mol H2,测得CO2的物质的量随时间变化如表所示.从反应开始到5min末,用CO2浓度变化表示的平均反应速率v(CO2)=0.05mol/(L.min);
反应达到平衡状态,此时H2的转化率为75%.
| t/min | 0 | 2 | 5 | 10 | 15 |
| n(CO2)/mol | 1 | 0.75 | 0.5 | 0.25 | 0.25 |
a.v生成(CH3OH)=v消耗(CO2)
b.CO2、H2、CH3OH、H2O的浓度均不再变化
c.n(CO2):n(H2):n(CH3OH):n(H2O)=1:1:1:1
d.H2的消耗速率与CH3OH的消耗速率之比为3:1.
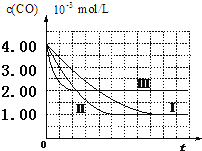 根据我国目前汽车业发展速度,预计2020年汽车保有量超过2亿辆,中国已成为全球最大的汽车市场.因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题.目前,汽车厂滴常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.
根据我国目前汽车业发展速度,预计2020年汽车保有量超过2亿辆,中国已成为全球最大的汽车市场.因此,如何有效处理汽车排放的尾气,是需要进行研究的一项重要课题.目前,汽车厂滴常利用催化技术将尾气中的NO和CO转化成CO2和N2,化学方程式如下:2NO+2CO$\frac{\underline{\;催化剂\;}}{\;}$2CO2+N2.为研究如何提高该转化过程反应速率,某课题组进行了以下实验探究.【资料查阅】①不同的催化剂对同一反应的催化效率不同;②使用相同的催化剂,当催化剂质量相等时,催化剂的比表面积对催化效率影响.
【实验设计】课题组为探究某些外界条件对汽车尾气转化反应速率的影响规律,设计了以下对比实验.
(1)完成以下实验设计表(表中不要留空格).
| 实验编号 | 实验目的 | T/℃ | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 同质量的同种催化剂的比表面积m2/g |
| Ⅰ | 为以下实验作参照 | 280 | 6.5×10-3 | 4.00×10-3 | 80 |
| Ⅱ | 探究同质量的同种催化剂的比表面积对尾气转化速率的影响 | 280 | 6.5×10-3 | 4.00×10-3 | 120 |
| Ⅲ | 探究温度对尾气转化速率的影响 | 360 | 6.5×10-3 | 4.00×10-3 | 80 |
(2)由图可知,第Ⅰ组实验中,CO的平衡浓度为1.00×10-3mol/L,计算达平衡时NO的浓度为3.5×10-3mol/L.
(3)由曲线Ⅰ、Ⅱ可知,增大催化剂比表面积,汽车尾气转化速率增大(填“增大”、“减小”、“无影响”).
| A. | 3 mol H2和1 mol N2 | |
| B. | 2 mol NH3和1 mol N2 | |
| C. | 2 mol N2和3 mol H2 | |
| D. | 0.1 mol NH3、0.9 mol N2、2.85 mol H2 |