题目内容
已知某氢氧化钠溶液中的Na+与H2O的个数之比为1:a,则可求出此溶液中NaOH的质量分数为 .
考点:溶液中溶质的质量分数及相关计算
专题:物质的量浓度和溶解度专题
分析:根据N=nNA可知,离子或分子数目与其物质的量成正比,根据钠离子和水分子个数可以计算氢氧化钠和水的质量,从而得出溶液的质量分数.
解答:
解:氢氧化钠溶液中Na+与H2O的个数之比为1:a,结合原子守恒知,NaOH与H2O的物质的量之比为1:a,
则氢氧化钠和水的质量之比为:m(NaOH):m(H2O)=(40g/mol×1):(18g/mol×a)=20:9a,
所以溶质NaOH的质量分数为:w=
×100%=
%,
故答案为:氢氧化钠的质量分数为
%.
则氢氧化钠和水的质量之比为:m(NaOH):m(H2O)=(40g/mol×1):(18g/mol×a)=20:9a,
所以溶质NaOH的质量分数为:w=
| 40 |
| 40+18a |
| 2000 |
| 20+9a |
故答案为:氢氧化钠的质量分数为
| 2000 |
| 20+9a |
点评:本题考查了物质的量的有关计算,题目难度不大,明确已知条件及各个物理量之间的关系是解本题关键,并灵活运用基本公式.

练习册系列答案
 互动课堂系列答案
互动课堂系列答案
相关题目
下列叙述不正确的是( )
| A、混合物没有固定的组成,所以混合物没有固定的熔沸点 |
| B、H2SO4只有在水溶液中才能导电,而NaCl在溶液中和熔融状态下都能导电 |
| C、弱电解质溶液中有溶质分子,但强电解质溶液中没有溶质分子 |
| D、水的汽化、液化与煤的气化和液化均属物理变化 |
氯仿可作为局部麻醉剂,常因保存不慎而被空气中的O2氧化,产生剧毒的气体-光气(COCl2):2CHCl3+O2→2COCl2+2HCl.下列说法正确的是( )
| A、上述反应属于取代反应 |
| B、检验氯仿是否变质可选用的试剂是AgNO3溶液 |
| C、CH2Cl2有两种结构,说明CH4是正四面体结构 |
| D、CHCl3是常见的有机溶剂,大量使用对环境无影响 |
下列金属冶炼的原理错误的是( )
A、Cu2S+O2
| ||||
B、Fe2O3+2Al
| ||||
C、MgO+CO
| ||||
D、2Cr+Al2O3
|
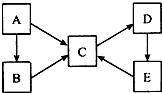 A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示:
A、B、C、D、E五种物质均含有同一种元素,它们之间的转化关系如图所示: