题目内容
如表为元素周期表的一部分,请回答有关问题:
(1)⑤的元素符号是 ;
(2)表中最活泼的金属是 ,非金属性最强的元素是 ;(填写元素符号)
(3)表中能形成两性氢氧化物的元素是 ,分别写出该元素的氢氧化物与⑥、⑨的最高价氧化物对应水化物反应的化学方程式 ; .
| ⅠA | ⅡA | ⅢA | ⅣA | VA | ⅥA | ⅦA | 0 | |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 4 | ⑨ | ⑩ |
(2)表中最活泼的金属是
(3)表中能形成两性氢氧化物的元素是
考点:元素周期表的结构及其应用,元素周期律和元素周期表的综合应用
专题:元素周期律与元素周期表专题
分析:(1)根据元素周期表,可确定①、②、③、④、⑤、⑥、⑦、⑧、⑨、⑩元素分别为:N、F、Mg、Al、Si、S、Cl、Ar、K、Br;
(2)又知金属性:同周期从左到右越来越小,同主族从上到下越来越大;而非金属性:同周期从左到右越来越大,同主族从上到下越来越小;
(3)氢氧化铝为两性化合物,既能与酸反应,又能与碱反应.
(2)又知金属性:同周期从左到右越来越小,同主族从上到下越来越大;而非金属性:同周期从左到右越来越大,同主族从上到下越来越小;
(3)氢氧化铝为两性化合物,既能与酸反应,又能与碱反应.
解答:
解:(1)从5在元素周期表中的位置第三周期第ⅣA族可知⑤为元素硅Si,故答案为:Si;
(2)表中最活泼的金属应从元素周期表的左下角去找⑨应为元素钾K.非金属性最强的元素应从元素周期表的右上角去找,②应为元素氟F,故答案为:K;F;
(3)表中能形成两性氢氧化物的元素是④元素铝Al,⑥元素为S最高价氧化物的水化物为H2SO4,它与Al(OH)3反应的化学方程式为:2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O以及Al(OH)3+KOH=KAlO2+2H2O,
故答案为:Al;2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;Al(OH)3+KOH=KAlO2+2H2O.
(2)表中最活泼的金属应从元素周期表的左下角去找⑨应为元素钾K.非金属性最强的元素应从元素周期表的右上角去找,②应为元素氟F,故答案为:K;F;
(3)表中能形成两性氢氧化物的元素是④元素铝Al,⑥元素为S最高价氧化物的水化物为H2SO4,它与Al(OH)3反应的化学方程式为:2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O以及Al(OH)3+KOH=KAlO2+2H2O,
故答案为:Al;2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O;Al(OH)3+KOH=KAlO2+2H2O.
点评:关于元素周期律的考题一般难度都不大,做好该类型题目的关键是要准.要在头脑中有一个完整准确的元素周期表,这样就能准确判断元素,尽而回答出相关的问题.该题设计实验虽然简单,但体现了新课标的要求.

练习册系列答案
相关题目
下列有关物质的性质和应用的说法中正确的是( )
| A、二氧化硫和氯水均具有漂白性,混合使用效果更好 |
| B、对滴有酚酞试液的CH3COONa溶液加热,溶液的颜色将变浅 |
| C、新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| D、用脱硫处理的煤代替原煤做燃料可以有效减少空气中CO2气体的含量 |
氯仿可作为局部麻醉剂,常因保存不慎而被空气中的O2氧化,产生剧毒的气体-光气(COCl2):2CHCl3+O2→2COCl2+2HCl.下列说法正确的是( )
| A、上述反应属于取代反应 |
| B、检验氯仿是否变质可选用的试剂是AgNO3溶液 |
| C、CH2Cl2有两种结构,说明CH4是正四面体结构 |
| D、CHCl3是常见的有机溶剂,大量使用对环境无影响 |
下列离子方程式正确的是( )
| A、小苏打溶液中加入醋酸:HCO3-+H+═CO2↑+H2O |
| B、碳酸氢铵溶液和足量氢氧化钠溶液混合:NH4++OH-═NH3?H2O |
| C、NaHS水解:HS-+H2O═S2-+H3O+ |
| D、硫酸亚铁溶液中滴加酸化的双氧水:2Fe2++2H++H2O2═2Fe3++2H2O |
设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A、1L 1mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| B、78g苯含有C=C双键的数目为3NA |
| C、标准状况下,6.72L NO2与水充分反应转移的电子数目为0.1NA |
| D、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
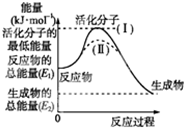 请认真观察图,然后回答问题.
请认真观察图,然后回答问题.