题目内容
4.W、X、Y、Z是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中 的两种或三种元素组成的化合物,己是由Y元素形成的单质,常温下丙和己均为气体.已知反应:甲+乙→丁+己,甲+丙→戊+己.又知常温下0.01mol•L-1丁溶液的pH为12.下列说法正确的是( )| A. | 元素X在周期表中的位置为第2周期VIA族 | |
| B. | 1 mol甲与足量的乙完全反应转移的电子数为6.02×1023 | |
| C. | 元素X、Y、Z的原子半径由大到小的顺序为r(Z)>r(Y)>r(x) | |
| D. | 1.0 L 0.1 mol•L-1戊溶液中阴离子的总物质的量小于0.1 mol |
分析 0.01 mol/L 丁溶液的pH为12,丁是一元强碱,其含有的金属元素在短周期,则丁应为NaOH,发生反应:甲+乙=丁+己,根据元素守恒可知,甲、乙两种物质至少共含有H、O、Na元素,己是由Y元素组成的单质,由发生反应可知,己不能是Na,结合原子数可知,W为H、Y为O、Z为Na元素,故己为氧气,可知甲是Na2O2、乙是水,再根据反应:甲+丙=戊+己,可知丙是二氧化碳,戊是碳酸钠,则Y为碳元素,结合对应单质、化合物的性质以及题目要求可解答该题.
解答 解:0.01 mol/L 丁溶液的pH为12,丁是一元强碱,其含有的金属元素在短周期,则丁应为NaOH,发生反应:甲+乙=丁+己,根据元素守恒可知,甲、乙两种物质至少共含有H、O、Na元素,己是由Y元素组成的单质,由发生反应可知,己不能是Na,结合原子数可知,W为H、Y为O、Z为Na元素,故己为氧气,可知甲是Na2O2、乙是水,再根据反应:甲+丙=戊+己,可知丙是二氧化碳,戊是碳酸钠,则Y为碳元素.
A.X为碳,在周期表中的位置为:第二周期第ⅣA族,故A错误;
B.甲与足量的乙完全反应的方程式为:2Na2O2+2H2O═4NaOH+O2↑,1molNa2O2反应转移的电子为1mol,约6.02×1O23个电子,故B正确;
C.同周期随原子序数增大原子半径减小,同主族自上而下原子半径增大,故原子半径大小顺序为:Na>C>O,即:r(Z)>r(X)>r(Y),故C错误;
D.戊是碳酸钠,在碳酸钠溶液中,CO32-离子水解生成HCO3-离子和OH-离子,溶液中阴离子总的物质的量大于0.1mol,故D错误,
故选B.
点评 本题为元素化合物推断,题目难度中等,需要学生熟练掌握元素化合物知识,“0.01mol•L-1丁溶液的pH为12”是推断突破口,对学生的逻辑推理有一定的要求,D选项注意盐类水解.

| A. | ②①③④ | B. | ②③④① | C. | ④②③① | D. | ④③①② |
| A. | V正=0 | B. | V逆=0 | C. | V正=V逆≠0 | D. | V正=V逆=0 |
| A. | 单质Se在空气中燃烧可生成SeO2 | B. | Se的原子序数为24 | ||
| C. | 可形成Na2SeO3、Na2SeO4两种盐 | D. | H2S比H2Se稳定 |
| A. | CuSO4溶液中加入过量氨水得到深蓝色溶液:Cu2++2OH-═Cu(OH)2↓ | |
| B. | 碳酸钠溶液中滴入酚酞试液,溶液变红:CO32-+2H2O?H2CO3+2OH- | |
| C. | FeCl2溶液中加入K3[Fe(CN)6]溶液,生成蓝色沉淀:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓ | |
| D. | 90℃时,测得纯水pH=6.7,pH<7的原因是:H2O(l)?H+(aq)+OH-(aq)△H<0 |
| 滴加试剂 | 蒸馏水 | 盐酸 | 氯化铵溶液 |
| 现象 |
 研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )
研究电化学腐蚀及防护的装置如图所示.下列有关说法错误的是( )| A. | d为石墨,铁片腐蚀加快 | |
| B. | d为石墨,石墨上电极反应为:O2+2H2O+4e-=4OH- | |
| C. | d为锌块,铁片不易被腐蚀 | |
| D. | d为锌块,铁片上电极反应为:2H++2e-→H2↑ |

 ;水杨酸与小苏打溶液反应的化学方程式:
;水杨酸与小苏打溶液反应的化学方程式: ; 一定条件下,C与F反应的反应类型是_酯化反应.
; 一定条件下,C与F反应的反应类型是_酯化反应. .
.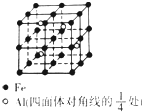 某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.
某宝石的主要成分是Al2O3,其中混有少量Mg、Ti、Fe等杂质而使其呈蓝色.