题目内容
下列说法正确的是( )
| A.需要加热方能发生的反应一定是吸热反应 |
| B.若反应为放热反应,则该反应不必加热就可发生 |
| C.放热反应比吸热反应容易发生 |
| D.化学反应都伴随着能量的变化 |
D
反应开始时需要加热的反应可能是吸热反应,也可能是放热反应,选项A、B错误;反应是放热还是吸热主要取决于反应物和生成物所具有的总能量的相对大小,而反应发生的难易程度与反应吸热还是放热无关。选项C错误;任何化学反应都伴随着能量的变化。

练习册系列答案
 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案
相关题目

 CH3OCH3(g) + 3H2O(g)
CH3OCH3(g) + 3H2O(g) O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )

 CO(g)+3H2(g)。该反应ΔH=+206 kJ·mol-1。
CO(g)+3H2(g)。该反应ΔH=+206 kJ·mol-1。 O2(g)
O2(g)  SO3(g)ΔH=-98.3 kJ·mol-1
SO3(g)ΔH=-98.3 kJ·mol-1 O2(g)
O2(g)  H2O(l) ΔH="-57.3" kJ·mol-1,回答下列问题。
H2O(l) ΔH="-57.3" kJ·mol-1,回答下列问题。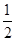 O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2
O2(g)=CO(g) ΔH1;C(s)+O2(g)=CO2(g) ΔH2