题目内容
(1)某反应过程中的能量变化如图所示:

写出该反应的热化学方程式: 。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,其热化学方程式为 。

写出该反应的热化学方程式: 。
(2)0.3 mol气态高能燃料乙硼烷(B2H6)在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5 kJ的热量,其热化学方程式为 。
(1)A(g)+2B(g)=C(l)+3D(l)ΔH=-432 kJ·mol-1
(2)B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)ΔH=-2 165 kJ·mol-1
(2)B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)ΔH=-2 165 kJ·mol-1
(1)由图可知,该反应为放热反应,然后据物质的状态和物质的量多少,以及热量的大小和单位,写出热化学方程式。
(2)0.3 mol B2H6燃烧放出热量为649.5 kJ,则1 mol B2H6燃烧放出2 165 kJ的热量。
(2)0.3 mol B2H6燃烧放出热量为649.5 kJ,则1 mol B2H6燃烧放出2 165 kJ的热量。

练习册系列答案
相关题目
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
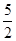 O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )
O2(g)=2CO2(g)+H2O(l) ΔH=-1300 kJ/mol 的说法中,正确的是( )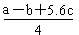
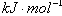
 2SO3(g)
2SO3(g)
 NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______
NH4++ NH2-,某温度时,其离子积K=2×l0-30。该温度下:①将少量NH4Cl固体加入液氨中,K____________2×10-30(填“<”、“>”或“=”);②将少量金属钠投入液氨中,完全反应后所得溶液中各微粒的浓度大小关系为:_______