题目内容
已知热化学方程式:SO2(g)+  O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
 O2(g)
O2(g)  SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )
SO3(g) △H = ―98.32kJ/mol,在容器中充入2molSO2和1molO2充分反应,最终放出的热量为( )| A.196.64kJ | B.196.64kJ/mol | C.<196.64kJ | D.>196.64kJ |
C
试题分析:根据题意可知1mol的SO2发生反应放出热量为98.32kJ。在容器中充入2molSO2和1molO2充分反应,由于该反应为可逆反应,所以最终反应消耗的SO2的物质的量比2mol少。所以最终放出的热量<2×98.32kJ=196.64kJ 。因此选项为C。

练习册系列答案
 发散思维新课堂系列答案
发散思维新课堂系列答案
相关题目
 O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol
O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol O2(g) = NO3-(aq) ΔH = -73kL/mol
O2(g) = NO3-(aq) ΔH = -73kL/mol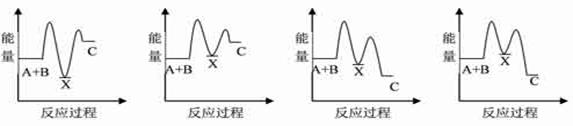
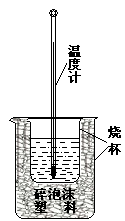
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
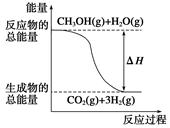
 O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1
O2(g)=CO2(g)+2H2(g) ΔH=-192.9 kJ·mol-1