题目内容
实验室用铜与稀硝酸制取NO时,为加快反应速率可采取的措施是
| A.增加铜的用量 | B.增大压强 |
| C.隔绝空气加热 | D.增大硝酸的浓度 |
C
解析试题分析:铜是固体,改变固体的质量,反应速率不变;铜和稀硝酸都不是气体,压强对该反应的反应速率不影响;隔绝空气加热,相当于是升高温度,反应速率加快;增大硝酸的浓度,有可能生成NO2,不正确,答案选C。
考点:考查外界条件对反应速率的影响
点评:该题是高考中的常见题型和重要的考点,主要是考查学生对影响反应速率因素的熟悉了解程度,旨在巩固学生的基础,提高学生的应试能力。该题的关键是注意外界条件对反应速率影响的适用范围,本题的易错点是选项D。

对于可逆反应2SO2+O2 2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子( )
2SO3,在混合气体中充入一定量的18O2,足够长的时间后,18O原子( )
| A.只存在于O2中 | B.只存在于O2和SO3中 |
| C.只存在于O2和SO2中 | D.存在于O2、SO2和SO3中 |
某温度下,在一个2L的密闭容器中,加入4molA和2molB进行如下反应:
3A(g)+2B(g) 4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
4C(?)+2D(?),反应一段时间后达到平衡,测得生成1.6molC,且反应的前后压强之比为5:4(相同的温度下测量),则下列说法正确的是( )
A.该反应的化学平衡常数表达式是K=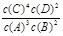 |
| B.此时,B的平衡转化率是35% |
| C.增大该体系的压强,平衡向右移动,化学平衡常数增大 |
| D.增加C,B的平衡转化率不变 |
将H2(g)和Br2(g)充入恒容密闭容器,恒温下发生反应H2(g)+Br2(g)  2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
2HBr(g)△H<0,平衡时Br2(g)的转化率为a;若初始条件相同,绝热下进行上述反应,平衡时Br2(g)的转化率为b。a与b的关系是
| A.a>b | B.a=b | C.a<b | D.无法确定 |
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应
TaS2(s)+2I2(g) TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
TaI4(g)+S2(g)△H=a kJ·mol-1 (I)
达平衡时,TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为3 mol 、2mol、2mol、2mol。
(1)反应(I)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”)。
(3)在不同温度下,该反应的平衡常数K如下表:
| 温度/℃ | 40 | 80 | 200 |
| 平衡常数K | 1 | 1.5 | 4 |
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 (写出计算过程,结果保留小数点后1位)
(15分)太阳能电池是利用光电效应实现能量变化的一种新型装置,目前多采用单晶硅和多晶硅作为基础材料。高纯度的晶体硅可通过以下反应获得:
反应①(合成炉):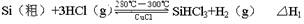
反应②(还原炉):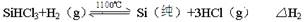
有关物质的沸点如下表所示:
| 物质 | BCl3 | PCl3 | SiCl4 | AsCl3 | AlCl3 | SiHCl3 |
| 沸点 | 12.1 | 73.5 | 57.0 | 129.4 | 180(升华) | 31.2 |
(1)太阳能电池的能量转化方式为 ;由合成炉中得到的SiHCl3往往混有硼、磷、砷、铝等氯化物杂质,分离出SiHCl3的方法是 。
(2)对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(cB)也可表示平衡常数(记作KP),则反应①的KP= ;
(3)对于反应②,在0.1Mpa下,不同温度和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如下表所示:

①该反应的△H2 0(填“>”、“<”、“=”)
②按氢气配比5:1投入还原炉中,反应至4min时测得HCl的浓度为0.12mol·L—1,则SiHCl3在这段时间内的反应速率为 。
③对上表的数据进行分析,在温度、配比对剩余量的影响中,还原炉中的反应温度选择在1100℃,而不选择775℃,其中的一个原因是在相同配比下,温度对SiHCl3 剩余量的影响,请分析另一原因是 。
(4)对于反应②,在1100℃下,不同压强和氢气配比(H2/SiHCl3)对SiHCl3剩余量的影响如图27—1所示:
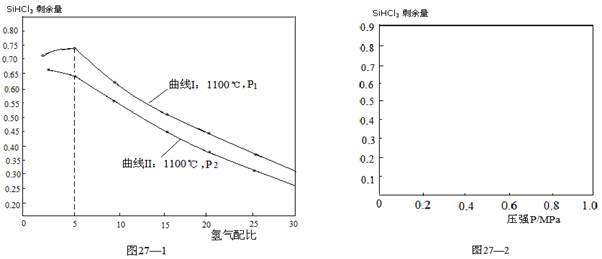
① 图中P1 P2(填“>”、“<”、“=”)
②在图27—2中画出氢气配比相同情况下,1200℃和1100℃的温度下,系统中SiHCl3剩余量随压强变化的两条变化趋势示意图。
 3C+4D中,表示该反应速率最快的是( )
3C+4D中,表示该反应速率最快的是( ) xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求:
xC(g)+2D(g),经5 min后,测得D的浓度为0.5 mol/L,c(A)∶c(B)=3∶5,C的平均反应速率为0.1 mol/(L·min)。求: 3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。
3C(g)+D(s),2分钟反应达到平衡,此时C的浓度为1.2 mol/L。