题目内容
2.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列有关说法正确的是( )| A. | 若mXa+与nYb-符合题目要求,则m+a=n-b | |
| B. | 若X的原子半径大于Y,则气态氢化物的稳定性HmX一定小于HnY | |
| C. | X,Y一定不是相邻周期元素 | |
| D. | 若X,Y处于同一周期且X离子所带电荷多于Y离子,则离子半径一定为:X>Y |
分析 A.简单离子的电子层结构相同,则核外电子数相同;
B.简单离子的电子层结构相同,X的原子半径大于Y,X可能为金属;
C.简单离子的电子层结构相同,X、Y均为阴离子、或均为阳离子在同一周期,否则不在同一周期;
D、电子层结构相同,核电荷数越多半径越小.
解答 解:A.由mXa+与nYb-,离子的电子层结构相同,则核外电子数相同,所以m-a=n+b,故A错误;
B.简单离子的电子层结构相同,X的原子半径大于Y,X可能为金属,则不存在气态氢化物,故B错误;
C.简单离子的电子层结构相同,X、Y均为阴离子、或均为阳离子在同一周期,若一个为阳离子一个为阴离子,则一定不在同一周期,故C错误;
D、电子层结构相同,核电荷数越多半径越小,X,Y处于同一周期且X离子所带电荷多于Y离子,所以Y的核电荷数多,所以离子半径一定为:X>Y,故D正确;
故选D.
点评 本题考查具有相同电子层结构的离子,明确X、Y可能为阴离子、阳离子及相对位置是解答本题的关键,题目难度不大.

练习册系列答案
相关题目
10.下列物质在给定条件下同分异构体数目正确的是( )
| A. | C4H10属于烷烃的同分异构体有3种 | |
| B. | 结构为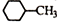 的一溴代物有5种 的一溴代物有5种 | |
| C. | 分子组成是C4H80属于醛类的同分异构体有3种 | |
| D. | 分子组成是C5H10O2属于羧酸的同分异构体有5种 |
7.下列说法正确的是( )
| A. | SiO2晶体易溶于水,水溶液呈现酸性 | |
| B. | CO2通入水玻璃中不可能得到硅酸 | |
| C. | SiO2是酸性氧化物,它不溶于任何酸 | |
| D. | SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑是制造玻璃的反应之一 |
14.一种从植物中提取的天然化合物,其结构为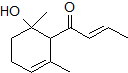 ,可用于制作香水.有关该化合物的下列说法正确的是( )
,可用于制作香水.有关该化合物的下列说法正确的是( )
 ,可用于制作香水.有关该化合物的下列说法正确的是( )
,可用于制作香水.有关该化合物的下列说法正确的是( )| A. | 分子式为C12H20O2 | B. | 该化合物可使酸性KMnO4溶液褪色 | ||
| C. | 该化合物可与NaOH溶液发生反应 | D. | 1 mol该化合物可与2 mol Br2加成 |
11.经测定,某溶液中只含有NH4+、Cl-、H+、OH-四种离子,下列说法中错误的是( )
| A. | 溶液中四种离子之间可能满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| B. | 若溶液中的溶质是NH4Cl和NH3•H2O,则不等式c(NH4+)>c(Cl-)>c(NH3•H2O)>c(H+)一定正确 | |
| C. | 若溶液中四种离子满足:c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中的溶质一定只有NH4Cl | |
| D. | 若溶液中c(Cl-)=c(NH4+),则该溶液呈中性 |
12.下列各组稀溶液:①氨水和硝酸银 ②NaAlO2和盐酸 ③硫酸氢钠和氢氧化钡 ④硝酸和碳酸钠.只用试管、滴管及闻气味就能鉴别的是( )
| A. | ③④ | B. | ①②④ | C. | ①②③④ | D. | ②④ |
 ,
,