题目内容
17.研究性学习小组的同学为了了解Cu及其化合物的性质,提出以下问题;①Al(OH)3具有两性,Cu(OH)2也具有两性吗?
②Fe的+2价化合物的稳定性比+3价化合物的稳定性小,Cu的+1价化合物的稳定性也比+2价化合物的稳定性小吗?
③CuO能被H2、CO等还原,也能被NH3还原吗?
(1)解决问题①需要用到的药品有CuSO4溶液、B、C(填字母).
A.A1Cl3溶液 B.NaOH溶液 C.稀H2SO4 D.H2O2溶液
假若Cu(OH)2具有两性,应该看到的实验现象是Cu(OH)2既能溶于稀硫酸,又能溶于NaOH溶液
(2)为了比较Cu的+1价化合物和+2价化合物的稳定性,他们取98gCu(OH)2固体,加热至800C~1000C时,得到黑色固体粉末,继续加热到10000C以上,黑色粉末全部变成红色粉末X.冷却后称量,X的质量为72g.向X中加入过量稀硫酸,得到蓝色溶液,同时观察到容器中还有红色固体存在.据此可推得,X的化学式为Cu2O,得出的结论是高于1000℃时Cu2O比CuO稳定在溶液中Cu2+比Cu+稳定.
(3)为解决问题③,设计了如图的实验装置(夹持及尾气处理装置未画出):
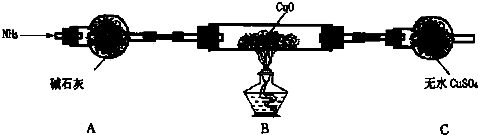
在实验中观察到CuO变成红色物质,无水CuSO4变成蓝色,生成物中还有一种无污染的单质气体.装置A的作用是干燥NH3,B中发生反应的化学方程式为3CuO+2NH3═3Cu+N2+3H2O.
分析 (1)要证明Cu(OH)2具有两性,应先加入碱生成Cu(OH)2,根据提供的药品可确定还需要的药品;
(2)根据在不同温度下反应物的组成可确定物质的稳定性;
(3)碱石灰,用来干燥氨气;CuO和NH3反应生成Cu、N2和H2O.
解答 解:(1)要证明Cu(OH)2具有两性,应先加入碱生成Cu(OH)2,根据提供的药品可确定还需要的药品;假若Cu(OH)2具有两性,应该看到的实验现象是Cu(OH)2既能溶于稀硫酸,又能溶于NaOH溶液,故答案为:BC; Cu(OH)2既能溶于稀硫酸,又能溶于NaOH溶液;
(2)加热到1000℃以上,黑色粉末全部变成红色粉末X,X的质量为72g,为氧化亚铜,根据在不同温度下反应物的组成可确定物质的稳定性,所以高于1000℃时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定,根据反应物和产物书写离子方程式Cu2O+2H+=Cu+Cu2++H2O,故答案为:Cu2O;高于1000℃时Cu2O比CuO稳定,在溶液中Cu2+比Cu+稳定;
(3)装置A盛有碱石灰,用来干燥氨气;CuO和NH3反应生成Cu、N2和H2O,方程式为3CuO+2NH3═3Cu+N2+3H2O,
故答案为:干燥NH3;3CuO+2NH3═3Cu+N2+3H2O.
点评 本题以实验探究的方式考查学生将金属铜及其化合物的性质,注意知识的迁移和应用,综合性较强,难度较大.

练习册系列答案
相关题目
5.在溶液中能大量共存,若加入OH-就有沉淀析出,若加入H+就能放出气体的是( )
| A. | Mg2+、Na+、Cl-、CO32- | B. | Ba2+、K+、OH-、NO3- | ||
| C. | H+、Al3+、NH4+、SO42- | D. | Na+、Cl-、Ca2+、HCO3- |
8. 粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
 粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )
粗铜中一般含有锌、铁、银、金等杂质.在如图所示的装置中,甲池的总反应方程式为:2CH3OH+3O2+4KOH═2K2CO3+6H2O.接通电路一段时间后,纯Cu电极质量增加了3.2g.在此过程中,下列说法正确的是( )| A. | 甲池中电解质溶液的pH值减小 | |
| B. | 乙池中CuSO4溶液的浓度不变 | |
| C. | 甲池中理论上消耗空气的体积是2.8L(空气中O2体积分数以20%计算) | |
| D. | 甲池通入CH3OH一极的电极反应为:CH3OH-6e-+2H2O═CO32-+8H+ |
5.将AgCl分别加入盛有:①5mL水;②6mL 0.5mol/L NaCl溶液;③10mL 0.2mol/L CaCl2溶液;④10mL 0.1mol/L AgNO3的烧杯中,均有固体剩余,各溶液中c(Ag+)从大到小的顺序排列正确的是( )
| A. | ④①②③ | B. | ④③②① | C. | ④①③② | D. | ②③①④ |
12. 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
 某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )
某温度时,AgCl(s)?Ag+(aq)+Cl-(aq)在水中的沉淀溶解平衡曲线如图所示.下列说法正确的是( )| A. | 加入AgNO3,可以使溶液由c点变到d点 | |
| B. | 加入少量水,平衡右移,Cl-浓度减小 | |
| C. | d点没有AgCl沉淀生成 | |
| D. | c点对应的Ksp等于a点对应的Ksp |
2.X、Y均为元素周期表中前20号元素,其简单离子的电子层结构相同,下列有关说法正确的是( )
| A. | 若mXa+与nYb-符合题目要求,则m+a=n-b | |
| B. | 若X的原子半径大于Y,则气态氢化物的稳定性HmX一定小于HnY | |
| C. | X,Y一定不是相邻周期元素 | |
| D. | 若X,Y处于同一周期且X离子所带电荷多于Y离子,则离子半径一定为:X>Y |
9.关于下列各装置图的叙述中,正确的是( )
| A. | 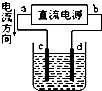 装置中,d为阳极、c为阴极 | |
| B. | 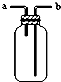 装置由a进气可用于收集H2、NH3、CO2、Cl2 等气体 | |
| C. | 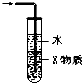 装置中X若为CCl4,可用于吸收NH3 或HCl,并可防止倒吸 | |
| D. | 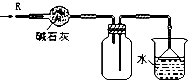 装置可用于干燥、收集HCl,并吸收多余的HCl |
6.用标准盐酸滴定未知浓度的NaOH溶液,下列有关实验操作的说法正确的是( )
| A. | 用蒸馏水洗净酸式滴定管后,装入标准盐酸进行滴定 | |
| B. | 用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,而后装入一定体积的NaOH溶液 | |
| C. | 滴定过程中视线应一直注视锥形瓶内混合液颜色的变化 | |
| D. | 用酚酞做指示剂,溶液由无色变浅红色,半分钟不变色为滴定终点 |
7.用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| B. | 标准状况下,22.4L己烷中共价键数目为19NA | |
| C. | 1L浓度为1 mol/L的Na2CO3溶液中含有NA个CO32- | |
| D. | 由CO2和O2组成的混合物中共有NA个分子,其中氧原子数为2NA |