题目内容
16.含有相同氧原子数的二氧化硫和三氧化硫,物质的量之比是3:2,质量之比比是6:5.把2mol/L CuSO4和1mol/L H2SO4溶液等体积混合(假设混合后溶液的体积等于混合前溶液的体积之和),求混合溶液中C(CuSO4)═1mol/L,C(SO42-)═1.5mol/L.分析 根据n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$计算,把2mol/L CuSO4和1mol/L H2SO4溶液等体积混合,假设体积为1L,分别计算物质的量,进而根据c=$\frac{n}{V}$计算浓度.
解答 解:含有相同氧原子数的SO2和SO3,分子数之比为3:2,由n=$\frac{m}{M}$=$\frac{N}{{N}_{A}}$可知,物质的量之比为3:2,则质量之比为3×64:2×80=6:5,
把2mol/L CuSO4和1mol/L H2SO4溶液等体积混合,假设体积为1L,则c(CuSO4)=$\frac{1L×2mol/L}{2L}$=1mol/L,c(SO42-)=$\frac{1L×2mol/L+1L×1mol/L}{2L}$=1.5mol/L.
故答案为:3:2;6:5;1;1.5.
点评 本题考查物质的量的计算,为高频考点,侧重于学生的分析、计算能力的考查,注意把握物质的构成特点以及相关计算公式的运用,难度不大.

练习册系列答案
相关题目
6.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 78g由Na2S和Na2O2组成的固体混合物,含有的阴离子数为NA | |
| B. | 标准状况下,22.4L CCl4中含有的分子数为NA | |
| C. | 将1mol FeCl3水解制成胶体,所得胶体中含有的胶体粒子数为NA | |
| D. | 1mol/L NaOH溶液中含有的Na+数目为NA |
7.下列各组中的离子,能在溶液中大量共存的是( )
| A. | H+、Ca2+、CO32-、Cl- | B. | H+、Fe2+、NO3-、OH- | ||
| C. | K+、Na+、Cl-、OH- | D. | Cu2+、Ba2+、Cl-、SO42- |
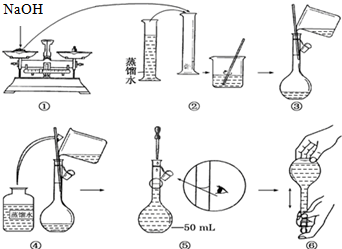
8.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.I配制0.50mol/L NaOH溶液
(1)若实验中大约要使用245mL NaOH溶液,则需要称量NaOH固体质量为:5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
(1)若实验中大约要使用245mL NaOH溶液,则需要称量NaOH固体质量为:5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 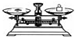 |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
5.室温下,向pH=13的氢氧化钡溶液中加入等体积的下列溶液后,滴入石蕊试液,出现蓝色,该溶液可能是( )
| A. | 0.05 mol•L-1的硫酸溶液 | B. | 0.1 mol•L-1的硫酸钠溶液 | ||
| C. | pH=1的醋酸溶液 | D. | pH=1的盐酸 |
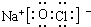 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+. Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.