题目内容
8.某实验小组用0.50mol/L NaOH溶液和0.50mol/L硫酸溶液进行中和热的测定.I配制0.50mol/L NaOH溶液(1)若实验中大约要使用245mL NaOH溶液,则需要称量NaOH固体质量为:5.0g.
(2)从图中选择称量NaOH固体所需要的仪器是(填字母):abe.
| 名称 | 托盘天平(带砝码) | 小烧杯 | 坩埚钳 | 玻璃棒 | 药匙 | 量筒 |
| 仪器 | 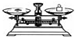 |  |  |  |  |  |
| 序号 | a | b | c | d | e | f |
分析 (1)依据使用溶液的体积,选择合适的容量瓶,依据M=CVM计算溶质的质量;
(2)氢氧化钠为腐蚀品要小烧杯中称量,结合托盘天平的使用方法选择称量固体氢氧化钠所用的仪器.
解答 解:(1)要使用245mL NaOH溶液,应选择250mL容量瓶,实际配制250mL0.50mol/L NaOH溶液溶液,需要氢氧化钠的质量m=0.25L×0.5mol/L×40g/mol=5.0g;
故答案为:5.0g;
(2)氢氧化钠要在称量瓶或者小烧杯中称量,称量固体氢氧化钠所用的仪器有天平、小烧杯和药匙,
故答案为:abe.
点评 本题考查了一定物质的量浓度溶液的配制,熟悉配制原理和容量瓶选择方法、托盘天平的使用方法是解题关键,题目难度不大.

练习册系列答案
相关题目
18.下列实验方案中,可行的是( )
| A. | 用氢氧化钠溶液除去CO2中的HCl气体 | |
| B. | 将白醋滴在湿润的pH试纸上,测定其pH | |
| C. | 按溶解、过滤、蒸发的操作顺序分离CaCl2、CaCO3的混合物 | |
| D. | 用BaCl2溶液除去KNO3溶液中少量的K2SO4 |
19.已知一种C(H+)=1×10-3mol•L-1的酸和一种C(OH-)=1×10-3mol•L-1的碱溶液等体积混合后溶液显碱性,其原因可能是( )
| A. | 浓的强酸和稀的强碱溶液反应 | |
| B. | 生成了一种强碱弱酸盐 | |
| C. | 浓的弱碱和稀的强酸溶液反应 | |
| D. | 等物质的量浓度的一元弱酸和一元强碱溶液反应 |
13.用托盘天平(指针向上的)称量样品时,若指针偏向右边,则表示( )
| A. | 左盘重,样品轻 | B. | 左盘轻,砝码重 | C. | 右盘重,砝码轻 | D. | 右盘轻重,样品重 |
17.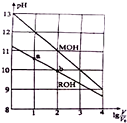 常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
 常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )
常温下,浓度均为0.10mol/L、体积均为V0的MOH和ROH溶液,分别加水稀释至体积V,pH随lg$\frac{V}{{V}_{0}}$的变化如图所示,下列叙述错误的是( )| A. | MOH的碱性强于ROH的碱性 | |
| B. | ROH的电离程度:b点大于a点 | |
| C. | 若两溶液无限稀释,则它们的c(OH-)相等 | |
| D. | 当lg$\frac{V}{{V}_{0}}$=2时,若两溶液同时升高温度,则$\frac{c({M}^{+})}{c({R}^{+})}$不变 |