题目内容
4.X、Y、Z、M四种短周期元素的原子半径依次减小.甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3;乙是日常生活的基础能源,其中含元素Y的质量分数为75%;丙是具有强氧化性的弱酸.丁为丙的钠盐,常用于漂白或消毒.戊与甲的组成元素相同,其分子具有18电子.请按要求回答下列问题:(1)元素X、Y的最高价氧化物的水化物的酸性由强到弱为(填化学式)HClO4>H2CO3;丁的电子式为
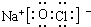 ;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+.
;与甲分子具有相同电子数且含元素种类相同的离子有(填化学式)OH-、H3O+.(2)元素E、F与X同周期.
①常温下E的单质与甲反应缓慢,加热至沸反应迅速,滴加酚酞试液,溶液变红色;此反应的化学方程式为Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$g(OH)2+H2↑.
②F的单质粉末加油漆后即得“银粉漆”,在汽车漆家族中有重要地位.写出保存“银粉”时的注意事项:密封、避免与酸或碱接触等.
(3)向盛有一定浓度戊溶液的烧杯中逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液.滴加过程中可依次观察到的现象:
a.浅绿色溶液变成黄色
b.有少量气泡产生,片刻后反应变得更剧烈,并放出较多热量
c.继续滴加溶液,静置一段时间,试管底部出现红褐色沉淀
①现象a中反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O;
②现象b中反应剧烈的化学方程式:2H2O2 $\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑;
③解释现象c:起始反应即①中使c(H+)降低,且反应②放热,使Fe3++3H2O
 Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
分析 X、Y、Z、M四种短周期元素的原子半径依次减小.甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3,甲为水,可推知M为H元素;丙是具有强氧化性的弱酸,则丙为HClO,乙是日常生活的基础能源,其中含元素Y的质量分数为75%,乙为甲烷,可推知X为Cl、Y为C元素、Z为O元素;丁为丙的钠盐,常用于漂白或消毒,则丁为NaClO;戊与甲的组成元素相同,其分子具有18电子,则戊为H2O2,据此解答.
解答 解:X、Y、Z、M四种短周期元素的原子半径依次减小.甲、乙、丙是由它们形成的三种常见分子;甲是人体必需的基本营养物质之一,约占人体体重的2/3,甲为水,可推知M为H元素;丙是具有强氧化性的弱酸,则丙为HClO,乙是日常生活的基础能源,其中含元素Y的质量分数为75%,乙为甲烷,可推知X为Cl、Y为C元素、Z为O元素;丁为丙的钠盐,常用于漂白或消毒,则丁为NaClO;戊与甲的组成元素相同,其分子具有18电子,则戊为H2O2.
(1)元素X、Y的最高价氧化物的水化物分别为:HClO4、H2CO3,非金属性Cl>C,故酸性由强到弱为HClO4>H2CO3;丁为NaClO,电子式为 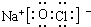 ;与甲(水)分子具有相同电子数且含元素种类相同的离子有:OH-、H3O+,
;与甲(水)分子具有相同电子数且含元素种类相同的离子有:OH-、H3O+,
故答案为:HClO4>H2CO3;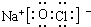 ;OH-、H3O+;
;OH-、H3O+;
(2)元素E、F与X(Cl)同周期.
①常温下E的单质与甲反应缓慢,加热至沸反应迅速,滴加酚酞试液,溶液变红色,则E为Mg,此反应的化学方程式为Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)2+H2↑,
故答案为:Mg+2H2O$\frac{\underline{\;\;△\;\;}}{\;}$g(OH)2+H2↑;
②F的单质粉末加油漆后即得“银粉漆”,则F为Al,易与氧气反应,与酸、碱反应,保存“银粉”时的注意密封、避免与酸或碱接触;
故答案为:密封;避免与酸或碱接触;
(3)①过氧化氢具有强氧化性,将亚铁离子氧化为铁离子,反应的离子方程式:2Fe2++H2O2+2H+=2Fe3++2H2O,故答案为:2Fe2++H2O2+2H+=2Fe3++2H2O;
②过氧化氢在铁离子作催化剂条件下分解生成水与氧气,反应方程式为:2H2O2 $\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑,
故答案为:2H2O2 $\frac{\underline{\;Fe_{3}+\;}}{\;}$2H2O+O2↑;
③起始反应即①使c(H+)降低,且反应②放热,使Fe3++3H2O Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀,
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀,
故答案为:起始反应即①中使c(H+)降低,且反应②放热,使Fe3++3H2O Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
Fe(OH)3+3H+△H>0,平衡正向移动,当水解出的Fe(OH)3较多时就聚集为沉淀.
点评 本题考查元素化合物推断,是对学生综合能力的考查,需要学生熟练注意元素化合物知识,难度中等.

 阅读快车系列答案
阅读快车系列答案| A. | 浓的强酸和稀的强碱溶液反应 | |
| B. | 生成了一种强碱弱酸盐 | |
| C. | 浓的弱碱和稀的强酸溶液反应 | |
| D. | 等物质的量浓度的一元弱酸和一元强碱溶液反应 |
| A. | 1molNa2CO3 | B. | 0.5molNa2CO3,0.5 molNa2O2 | ||
| C. | 0.25molNa2CO3,0.75 molNa2O2 | D. | O.75 molNa2CO3,0.25 molNa2O2 |
| A. | 左盘重,样品轻 | B. | 左盘轻,砝码重 | C. | 右盘重,砝码轻 | D. | 右盘轻重,样品重 |
| A. | 1.0 mol.L-l的NaAl02溶液和2.5 mol.L-l的盐酸等体积混合:2AlO${\;}_{2}^{-}$+5H+═Al(OH)3↓+Al3++H2O | |
| B. | 铜溶于0.5 mol.L-1的硝酸中:Cu+4H++2NO${\;}_{3}^{-}$═Cu2++2NO2↑+2H2O | |
| C. | 工业上将Cl2通人石灰乳中制漂白粉:Cl2+2OH-═Cl-+ClO-+H2O | |
| D. | 向Ba(OH)2溶液中加入少量的NH4HSO4溶液:Ba2++OH-+H++Si${\;}_{4}^{2-}$═BaSO4↓+H2O |