题目内容
8.下列说法中正确的是( )| A. | 向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象 | |
| B. | 检验某溶液是否含有SO${\;}_{4}^{2-}$时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 向100ml1mol/L的Ca(HCO3)2 溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱 |
分析 A.向饱和Na2CO3溶液中通入过量的CO2,生成NaHCO3,溶液变浑浊;
B.硫酸根离子检验应排除碳酸根、银离子、亚硫酸根离子干扰;
C.氢氧化钠固体溶于水放热;
D.向100ml1mol/L的Ca(HCO3)2溶液中加入等浓度等体积的NaOH溶液,生成CaCO3和NaHCO3.
解答 解:A.向饱和Na2CO3溶液中通入过量的CO2,生成NaHCO3,溶液变浑浊,故A错误;
B.硫酸根离子检验应排除碳酸根、银离子、亚硫酸根离子干扰,应先加入盐酸酸化,再加入氯化钡,故B错误;
C.氢氧化钠固体溶于水放热,将4g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出的热量大于5.73kJ,故C错误;
D.向100ml1mol/L的Ca(HCO3)2溶液中加入等浓度等体积的NaOH溶液,发生:Ca(HCO3)2+NaOH=CaCO3↓+NaHCO3+H2O,溶液HCO3-浓度减小,水解生成OH-的浓度减小,溶液的碱性减弱,故D正确;
故选:D.
点评 本题考查了碳酸盐的性质、硫酸根离子的检验、热化学方程式的含义,题目难度不大,注意离子检验应排除杂质离子的干扰.

练习册系列答案
相关题目
18.下列反应中,既是离子反应,又属于有颜色变化的氧化还原反应的是( )
| A. | 硫酸铁溶液和氢氧化钠溶液混合 | B. | 钠块投人水中 | ||
| C. | HCl和 NH3反应生成NH4Cl固体 | D. | 酸性 KMnO4溶液中通人 SO2气体 |
3.下列说法中正确的是( )
| A. | Fe2O3呈红棕色,可用做红色颜料 | |
| B. | 浓硫酸能腐蚀金属,不能用任何金属容器盛装浓硫酸 | |
| C. | 氯气有毒,利用这一性质可进行自来水的杀菌消毒 | |
| D. | 镁、铝都比较软,不能用做装饰材料 |
20.下列说法正确的是( )
| A. | 苯分子中不存在碳碳双键,所以不能发生加成反应 | |
| B. | 乙醇能发生氧化反应,乙酸则不可能发生氧化反应 | |
| C. | 乙酸和乙醇制乙酸乙酯与苯甲酸乙酯水解制苯甲酸和乙醇都属于取代反应 | |
| D. | 甲苯与氯气在光照下反应主要生成2,4-二氯甲苯 |
18.电子层数相同的三种元素X、Y、Z,它们最高价氧化物对应水化物的酸性由强到弱顺序为:HXO4>H2YO4>H3ZO4,下列判断不正确的是( )
| A. | 原子半径X>Y>Z | |
| B. | 气态氢化物稳定性X>Y>Z | |
| C. | 元素原子得电子能力由强到弱X>Y>Z | |
| D. | 单质与氢气反应由易到难X>Y>Z |
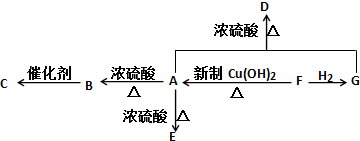
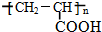 、GCH3CH(OH)CH2OH;
、GCH3CH(OH)CH2OH;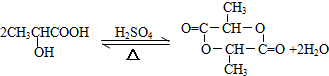 ;②F→A
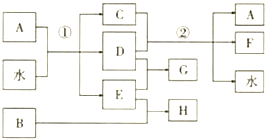
;②F→A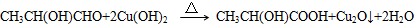 .
.
 ;
;