题目内容
18.下列反应中,既是离子反应,又属于有颜色变化的氧化还原反应的是( )| A. | 硫酸铁溶液和氢氧化钠溶液混合 | B. | 钠块投人水中 | ||
| C. | HCl和 NH3反应生成NH4Cl固体 | D. | 酸性 KMnO4溶液中通人 SO2气体 |
分析 离子反应,应能在溶液中进行,且有离子参加反应,氧化还原反应的特征是有化合价的升降,结合溶液的颜色解答该题.
解答 解:A.生成红褐色氢氧化铜,为复分解反应,故A错误;
B.生成氢氧化钠和氢气,为离子反应和氧化还原反应,但没有颜色变化,故B错误;
C.不是氧化还原反应,故C错误;
D.高锰酸钾和二氧化硫发生氧化还原反应,溶液颜色褪色,故D正确.
故选D.
点评 本题考查氧化还原反应,题目难度不大,注意把握离子反应以及氧化还原反应的实质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
11.下列关于化学腐蚀与电化学腐蚀的说法中,错误的是( )
| A. | 均是被腐蚀的金属失去电子的过程 | |
| B. | 均是需要有氧气参加的反应 | |
| C. | 化学腐蚀与电化学腐蚀往往是同时发生的 | |
| D. | 电化学腐蚀比化学腐蚀的速率通常情况下大得多 |
9.已知维生素A 的结构简式可写为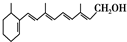 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
 ,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )
,式中以线示键,线的交点与端点处代表碳原子,并用氢原子数补足四价,但C、H原子未标记出来,关于它的叙述正确的是( )| A. | 维生素A的分子式为C20H30O | |
| B. | 维生素A中含有苯环 | |
| C. | 维生素A中可以使溴水褪色 | |
| D. | 1mol维生素A在催化剂作用下最多可与7molH2发生加成反应 |
6.下列工业生产过程中不涉及氧化还原反应的是( )
①制水泥、玻璃 ②制硝酸 ③制硫酸 ④氯碱工业 ⑤合成氨 ⑥制漂白粉 ⑦制皂.
①制水泥、玻璃 ②制硝酸 ③制硫酸 ④氯碱工业 ⑤合成氨 ⑥制漂白粉 ⑦制皂.
| A. | ①②③⑤ | B. | ①③⑤⑥⑦ | C. | 只有①⑦ | D. | ③⑥⑦ |
13.下列化学反应的离子方程式正确的是( )
| A. | 向FeCl3溶液中加入Cu粉:2Fe3++3Cu═2Fe+3Cu2+ | |
| B. | Cu和稀硝酸反应:Cu+2H++NO3-═Cu2++NO↑+H2O | |
| C. | NaOH溶液中通入少量二氧化硫:SO2+2OH-═SO32-+H2O | |
| D. | 碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
3.下列各组物质中都有两组分,两组分各取 1mol,在足量氧气中燃烧,两者消耗氧气的物质的量相同的是( )
| A. | 乙烯和乙醇 | B. | 甲醇和乙醛 | C. | 丁烷和乙酸乙酯 | D. | 葡萄糖和乙酸 |
10.下列说法正确的是( )
| A. | 2CH2=CH2+O2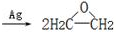 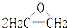 是理想的原子经济,原子利用率为100% 是理想的原子经济,原子利用率为100% | |
| B. | 含磷合成洗涤剂易被细菌分解,故不会导致水体污染 | |
| C. | CO2的大量排放能破坏臭氧层,形成“臭氧空洞” | |
| D. | pH在5.6~7.0之间的降水通常称为酸雨 |
7.在酸性的无色溶液中可大量共存的离子组是( )
| A. | Na+、OH-、Cl- | B. | Na+、NH4+、Cl- | C. | Cu2+、K+、Cl- | D. | K+、SO32-、ClO- |
8.下列说法中正确的是( )
| A. | 向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象 | |
| B. | 检验某溶液是否含有SO${\;}_{4}^{2-}$时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 向100ml1mol/L的Ca(HCO3)2 溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱 |