题目内容
3.下列说法中正确的是( )| A. | Fe2O3呈红棕色,可用做红色颜料 | |
| B. | 浓硫酸能腐蚀金属,不能用任何金属容器盛装浓硫酸 | |
| C. | 氯气有毒,利用这一性质可进行自来水的杀菌消毒 | |
| D. | 镁、铝都比较软,不能用做装饰材料 |
分析 A.Fe2O3是红棕色粉末,常用作红色涂料;
B.常温下,浓硫酸遇到铁铝发生钝化;
C.氯气与水反应生成次氯酸,所以氯气可用于自来水的杀菌消毒;
D.镁铝合金的硬度大,密度小,适合做装饰材料.
解答 解:A.Fe2O3是红棕色粉末,常用作红色涂料,故A正确;
B.浓硫酸具有强的氧化性,常温下能够使铁铝钝化,可以用铁铝容器盛放浓硫酸,故B错误;
C.氯气与水反应生成次氯酸,所以氯气可用于自来水的杀菌消毒,真正起作用的是氯气与水反应生成的次氯酸,故C错误;
D.镁铝形成的合金的硬度大,密度小,适合做装饰材料,故D错误;
故选:A.
点评 本题考查了物质的用途,熟悉物质的性质是解题关键,题目难度不大,注意合金的性质.

练习册系列答案
 金博士一点全通系列答案
金博士一点全通系列答案
相关题目
13.下列化学反应的离子方程式正确的是( )
| A. | 向FeCl3溶液中加入Cu粉:2Fe3++3Cu═2Fe+3Cu2+ | |
| B. | Cu和稀硝酸反应:Cu+2H++NO3-═Cu2++NO↑+H2O | |
| C. | NaOH溶液中通入少量二氧化硫:SO2+2OH-═SO32-+H2O | |
| D. | 碳酸氢钙溶液和氢氧化钠溶液混合:HCO3-+OH-═CO32-+H2O |
14.下列化学式与其名称的对应关系正确的是( )
| A. | 软脂酸 C17H33COOH | B. | 纯碱 Na2CO3•10H2O | ||
| C. | 纤维素[C6H7O2(OH)3]n | D. | 丙氨酸 CH2(NH2)CH2COOH |
18.下列与有机物的结构、性质有关的叙述正确的是( )
| A. | 苯、油脂均不能使酸性KMnO4溶液褪色 | |
| B. | 淀粉、纤维素、油脂和蛋白质均是高分子化合物 | |
| C. | 乙酸和乙醛可用新制的Cu(OH)2悬浊液加以区别 | |
| D. | 乙醇、乙酸能与Na反应放出H2,二者分子中官能团相同 |
8.下列说法中正确的是( )
| A. | 向饱和Na2CO3溶液中通入过量的CO2,溶液中无明显现象 | |
| B. | 检验某溶液是否含有SO${\;}_{4}^{2-}$时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 | |
| C. | 已知H+(aq)+OH-(aq)═H2O(l);△H=-57.3 kJ/mol.将4 g氢氧化钠固体放入100mL1mol/L的稀盐酸中,放出了5.73 kJ的热量 | |
| D. | 向100ml1mol/L的Ca(HCO3)2 溶液中加入等浓度等体积的NaOH溶液,溶液的碱性减弱 |
15. 下列两种方案制备氢氧化铝:
下列两种方案制备氢氧化铝:
Ⅰ:2.7gAl$\stackrel{100mL稀盐酸}{→}$X溶液$\stackrel{氢氧化钠溶液}{→}$氢氧化铝
Ⅱ2.7gAl$\stackrel{100mL氢氧化钠溶液}{→}$Y溶液$\stackrel{稀盐酸}{→}$氢氧化铝
已知所用的稀盐酸与氢氧化钠溶液均为3mol/L.图是向X溶液与Y溶液中分别加入氢氧化钠溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.(混合后体积变化忽略不计)下列说法正确的是( )
 下列两种方案制备氢氧化铝:
下列两种方案制备氢氧化铝:Ⅰ:2.7gAl$\stackrel{100mL稀盐酸}{→}$X溶液$\stackrel{氢氧化钠溶液}{→}$氢氧化铝
Ⅱ2.7gAl$\stackrel{100mL氢氧化钠溶液}{→}$Y溶液$\stackrel{稀盐酸}{→}$氢氧化铝
已知所用的稀盐酸与氢氧化钠溶液均为3mol/L.图是向X溶液与Y溶液中分别加入氢氧化钠溶液或稀盐酸时产生沉淀的质量与加入溶液体积之间的关系.(混合后体积变化忽略不计)下列说法正确的是( )
| A. | 在a曲线表示的是向Y溶液中加入稀盐酸 | |
| B. | 方案Ⅱ比方案Ⅰ生成更多的气体 | |
| C. | 在M点时,两方案中所得溶液的溶质质量分数相同 | |
| D. | M点以后,a、b两条曲线将重合为一条 |
12.下列关于化学用语表示正确的是( )
| A. | 四氯化碳电子式: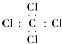 | |
| B. | 质子数35、中子数45的溴原子:${\;}_{35}^{80}$Br | |
| C. | 硫离子结构示意图: | |
| D. | HClO的结构式:H-Cl-O |
13.(1)为了达到下表中的实验要求,请从“供选择的化学试剂及方法”栏中,选择正确选项的字母代号填入对应的空格中.
(2)A的结构简式如下:A分子中两种含氧官能团的名称是羟基、羧基.

请写出该物质与足量的金属钠发生反应的化学方程式 +4Na→
+4Na→ +2H2↑.
+2H2↑.
| 序号 | 实验要求 | 答案 | 供选择的化学试剂及方法 |
| a | 检验乙酸是否具有酸性 | A.新制的氢氧化铜悬浊液 | |
| b | 检验植物油中是否含有碳碳双键 | B.紫色石蕊试液 | |
| c | 检验尿液中是否含有葡萄糖 | C.加入饱和Na2CO3溶液,分液 | |
| d | 除去乙酸乙酯中的少量乙酸 | D.溴水 |

请写出该物质与足量的金属钠发生反应的化学方程式
 +4Na→
+4Na→ +2H2↑.
+2H2↑.