题目内容
5.1,3-丙二醇是生产新型高分子材料PTT的主要原料,目前1,3-丙二醇的生产的路线有:以石油裂解气为原料的两条石化合成路线和一条生物工程法合成路线.【路线1】丙烯醛水合氢化法:

【路线2】环氧乙烷甲酰化法:

【路线3】生物发酵法:淀粉$\stackrel{酶}{→}$甘油$\stackrel{酶}{→}$1,3丙二醇
(1)从合成原料来源可持续性的角度看,你认为最具有发展前景的路线是3(填1、2或3).
(2)A的结构简式为CH2OHCH2CHO.
(3)路线2中
 反应类型为氧化反应.
反应类型为氧化反应.(4)环氧乙烷(
 )的核磁共振氢谱有1个信号峰,试写出与其互为同分异构体且核磁共振氢谱有
)的核磁共振氢谱有1个信号峰,试写出与其互为同分异构体且核磁共振氢谱有2个信号峰的有机物的结构简式CH3CHO.
(5)以1,3-丙二醇与对苯二甲酸(
 )为原料可以合成聚酯PTT,写出其化学方程式
)为原料可以合成聚酯PTT,写出其化学方程式 .
.(6)已知丙二酸二乙酯能发生以下反应:

利用该反应原理,以丙二酸二乙酯、1,3-丙二醇、乙醇为原料合成
 ,请你设计出合理的反应流程图
,请你设计出合理的反应流程图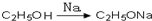 、
、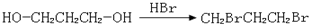 、
、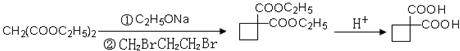 .提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A$→_{反应条件}^{反应物}$ B$→_{反应条件}^{反应物}$ C …
.提示:①合成过程中无机试剂任选,②合成反应流程图表示方法示例如下:A$→_{反应条件}^{反应物}$ B$→_{反应条件}^{反应物}$ C …
分析 (1)根据原料的是否为可再生资源进行判断;
(2)A与氢气发生加成反应生成1,3-丙二醇,A中含有不饱和键,环氧乙烷与CO、氢气发生加成反应生成A,A中含有-CHO,丙烯醛转化为A,应是与水发生加成反应,故A为HOCH2CH2CHO;
(3)该反应中,反应物得到氧元素生成产物,故该反应为氧化反应;
(4)核磁共振氢谱有2个信号峰,说明有机物分子中含有两个等效H,结合环氧乙烷的结构简式写出满足条件的有机物的结构简式;
(5)1,3-丙二醇与对苯二甲酸可发生缩聚反应,以此可书写反应的化学方程式;
(6)根据题意,应先生成C2H5ONa和CH2BrCH2CH2Br,然后与丙二酸二乙酯反应可生成目标物.
解答 解:(1)绿色化学是当下潮流,需要考虑可持续的资源再生问题,路线3以可再生资源淀粉为原料,路线1、2的原料为石油产品,而石油是不可再生资源,所以最具有发展前景的路线是3,
故答案为:3;
(2)A与氢气发生加成反应生成1,3-丙二醇,A中含有不饱和键,环氧乙烷与CO、氢气发生加成反应生成A,A中含有-CHO,丙烯醛转化为A,应是与水发生加成反应,故A的结构简式为:HOCH2CH2CHO,
故答案为:CH2OHCH2CHO;
(3)反应 中,反应物得到氧元素,所以该反应属于氧化反应,
中,反应物得到氧元素,所以该反应属于氧化反应,
故答案为:氧化反应;
(4)环氧乙烷( )的核磁共振氢谱有1个信号峰,其互为同分异构体且核磁共振氢谱有2个信号峰,说明该有机物分子中含有2个等效H,结合环氧乙烷的不饱和度可知,满足条件的有机物的结构简式为:CH3CHO,
)的核磁共振氢谱有1个信号峰,其互为同分异构体且核磁共振氢谱有2个信号峰,说明该有机物分子中含有2个等效H,结合环氧乙烷的不饱和度可知,满足条件的有机物的结构简式为:CH3CHO,
故答案为:CH3CHO;
(5)1,3-丙二醇与对苯二甲酸可发生缩聚反应,反应的化学方程式为: ,
,
故答案为: ;
;
(6)根据题意,应先生成C2H5ONa和CH2BrCH2CH2Br,然后与丙二酸二乙酯反应可生成目标物,发生反应的过程为:①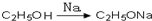 、②
、②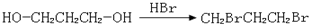 、③
、③ ,
,
故答案为: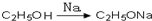 、
、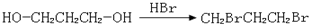 、
、 .
.
点评 本题考查有机合成,题目难度中等,(6)为易错点,理解题目给予的信息是关键,解答题目的时候注意把握官能团的结构和性质,根据官能团的变化进行分析,试题侧重考查学生的分析、理解能力及灵活应用基础知识的能力.

| A. | 为了让食品保存得更长一些,可以多加一些添加剂 | |
| B. | 在国家卫生部门规定的范围内使用食品添加剂,一般认为对人体无害 | |
| C. | 染衣服的染料也可以用给食品染色 | |
| D. | 某腌制的肉类颜色鲜红,说明该食品既新鲜又安全 |
| A. | CO2和SiO2 | B. | NaCl和HCl | ||
| C. | (NH4)2CO3和CO(NH2)2 (尿素) | D. | NaH和KCl |
| A. | 碳、氮原子构成网状的原子晶体 | |
| B. | 膜中的C-N键长比金刚石的C-C键长短 | |
| C. | 碳、氮都是非金属,化合时放出大量热 | |
| D. | 相邻主族非金属的化合物比单质硬度大 |
| A. | 沉淀X的成分是SiO2、Fe2O3 | |
| B. | 从蛇纹石组成看,其成分皆是碱性氧化物 | |
| C. | 溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+ | |
| D. | 在溶液Y中加入过量的氨水,过滤得到的沉淀是Al(OH)3、Fe(OH)3和Mg(OH)2 |
| A. | 电解硫酸时,阴极产生1molH2时,阳极一定产生0.5molO2 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5mol | |
| C. | 电解1mol熔融的Al2O3,能产生33.6L氧气、54.0g金属铝 | |
| D. | 工业用电解法进行粗铜精炼时,每转移1mol电子,阳极上就溶解0.5NA个铜原子 |
| A. | 硅酸钠的水溶液俗称水玻璃,可用作木材防火剂 | |
| B. | 开发核能、太阳能等新能,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放 | |
| C. | 用聚合硫酸铁作为净水剂,该处理过程中仅发生了化学变化 | |
| D. | 汽车尾气中含有氮的氧化物,是汽油不完全燃烧造成的 |

 .
. A、B、C、X是中学化学常见物质,它们在一定条件下具有如下转化关系:A+X→B+C+H2O
A、B、C、X是中学化学常见物质,它们在一定条件下具有如下转化关系:A+X→B+C+H2O