题目内容
9.氨的合成是最重要的化工生产之一.Ⅰ.合成氨用的氢气有多种制取的方法:
①活泼金属(如钠)直接跟水反应;
②金属(如锌)跟稀盐酸或稀硫酸反应;
③电解水制氢气
④由焦炭跟水反应制取氢气:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
⑤由天然气制取氢气:CH4+H2O(g)$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CO+3H2
(1)请你再补充一种制取氢气的方法,写出该反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(2)已知有关反应的能量变化如图,则方法⑤反应的焓变△H=(a+3b-c)kJ•mol-1.

Ⅱ.在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)$\frac{\underline{\;高温高压\;}}{催化剂}$2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 | 2mol NH3 |
| 达到平衡的时间(min) | 5 | 8 | |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | |
| NH3的体积分数 | ω1 | ω3 | |
| 混合气体密度(g•L-1) | ρ1 | ρ2 |
a.2c1>1.5mol/L b.2ρ1=ρ2 c.ω3=ω1
(4)在该温度下该反应的平衡常数K=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}×(3{c}_{1}-1.5)^{3}}$(用含c1的代数式表示).
(5)容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol/(L.min).
Ⅲ.用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)?CO (NH2)2(l)+H2O(g).某温度下,为进一步提高CO2的平衡转化率,下列措施中能达到目的是ab.
a.提高NH3的浓度 b.增大压强 c.及时转移生成的尿素 d.使用更高效的催化剂.
分析 I.(1)Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,可以制备氢气;
(2)由图可知,热化学方程式:
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H1=-akJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-bkJ•mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-ckJ•mol-1
根据盖斯定律,③-①-②×3可得:CH4(g)+H2O(g)=CO(g)+3H2(g),则△H=△H3-△H1-3△H2;
Ⅱ(3)a.乙等效为在在甲基础上压强增大一倍,平衡正向移动,平衡时乙中反应物转化率比甲中大;
b.乙中混合气体总质量为甲中2倍,容器容积均为2L,密度之比等于气体质量之比;
c.丙等效为在甲平衡的基础上移走1mol氮气到达的平衡,平衡时氨气的体积分数不同;
(4)计算平衡时各组分浓度,代入平衡常数表达式K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$计算;
(5)乙容器5min到达平衡,平衡时氮气浓度为1.5mol/L,计算氮气浓度变化量,根据v=$\frac{△c}{△t}$计算v(N2),再根据速率之比等于化学计量数之比计算v(H2);
Ⅲ.a.提高NH3的浓度,平衡正向移动;
b.正反应为气体体积减小的反应,增大压强,平衡正向移动;
c.尿素为液体,及时转移生成的尿素,不影响平衡移动;
d.使用更高效的催化剂,加快反应速率,不影响平衡移动.
解答 解:Ⅰ.(1)Al与氢氧化钠溶液反应生成偏铝酸钠与氢气,可以制备氢气,反应方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑,
故答案为:2Al+2NaOH+2H2O=2NaAlO2+3H2↑;
(2)由图1、图2、图3可分别得热化学方程式:
①CO(g)+$\frac{1}{2}$O2(g)=CO2(g)△H1=-akJ•mol-1
②H2(g)+$\frac{1}{2}$O2(g)=H2O(g)△H2=-bkJ•mol-1
③CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H3=-ckJ•mol-1
根据盖斯定律,由③-①-②×3可得:CH4(g)+H2O(g)═CO(g)+3H2(g),则△H=△H3-△H1-3△H2=(a+3b-c)kJ•mol-1,
故答案为:(a+3b-c)kJ•mol-1;
Ⅱ.(3)a.乙等效为在在甲基础上压强增大一倍,平衡正向移动,平衡时乙中反应物转化率比甲中大,则2c1>1.5mol/L,故a正确;
b.乙中混合气体总质量为甲中2倍,容器容积均为2L,密度之比等于气体质量之比,则2ρ1=ρ2,故B正确;
c.丙等效为在甲平衡的基础上移走1mol氮气到达的平衡,平衡时氨气的体积分数不同,故c错误;
故选:ab;
(4)甲容器到达平衡,平衡时氮气浓度为c1mol/L,则:
N2(g)+3H2(g)?2NH3(g)
起始量(mol/L):1 1.5 0
变化量(mol/L):1-c1 3(1-c1 ) 2(1-c1 )
平衡量(mol/L):c1 (3c1-1.5)2(1-c1 )
故平衡常数K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}×(3{c}_{1}-1.5)^{3}}$,
故答案为:$\frac{(2-2{c}_{1})^{2}}{{c}_{1}×(3{c}_{1}-1.5)^{3}}$;
(5)乙容器5min到达平衡,平衡时氮气浓度为1.5mol/L,则v(N2)=$\frac{\frac{4mol}{2L}-1.5mol/L}{5min}$=0.1mol/(L.min),速率之比等于化学计量数之比,v(H2)=3v(N2)=0.3mol/(L.min),
故答案为:0.3mol/(L.min);
Ⅲ.a.提高NH3的浓度,平衡正向移动,CO2的平衡转化率增大,故a正确;
b.增大压强,平衡正向移动,CO2的平衡转化率增大,故b正确;
c.尿素为液体,及时转移生成的尿素,不影响平衡移动,CO2的平衡转化率不变,故c错误;
d.使用更高效的催化剂,缩短到达平衡时间,不影响平衡移动,CO2的平衡转化率不变,故d错误,
故选:ab.
点评 本题考查化学平衡计算与影响因素、反应速率、平衡常数、反应热计算等,侧重于学生的分析能力和计算能力的考查,难度中等.

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案| 湿法 | 强碱性介质中,Fe(NO3)3与NaClO反应生成紫红色高铁酸盐溶液 |
| 干法 | Fe2O3、KNO3、KOH混合加热共熔生成紫红色高铁酸盐和KNO2等产物 |
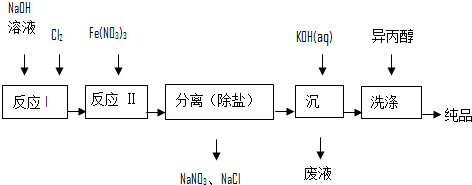
①洗涤粗品时选用异丙醇而不用水的理由是:减少高铁酸钾的溶解损失.
②反应Ⅰ的离子方程式为Cl2+20H-=Cl-+ClO-+H2O.
③反应Ⅱ中氧化剂与还原剂之比为3:2.
④已知25℃时Fe(OH)3的Ksp=4.0×10-38,反应Ⅱ后的溶液中c(Fe3+)=4.0×10-5 mol/L,则需要调整pH=3时,开始生成Fe(OH)3(不考虑溶液体积的变化).
(2)由流程图可见,湿法制备高铁酸钾时,需先制得高铁酸钠,然后再向高铁酸钠中加入饱和KOH溶液,即可析出高铁酸钾.
①加入饱和KOH溶液的目的是:增大K+浓度,促进高铁酸钾晶体析出.
②由以上信息可知:高铁酸钾的溶解度比高铁酸钠小(填“大”或“小”).
(3)请写出干法制备K2FeO4的化学反应方程式Fe2O3+3KNO3+4KOH=2K2FeO4+3KNO2+2H2O.
| A. | 0.45mol | B. | 0.8mol | C. | 0.9mol | D. | 1.2mol |
| A. | 反应在tmin内的平均速率为v(D)=0.4/tmol•L-1•min-1 | |
| B. | 温度升至500℃时,上述反应平衡常数为0.64,则正反应为吸热反应 | |
| C. | 保持其他条件不变,向平衡体系中再通入0.2molB,与原平衡相比,达到新平衡时A转化率增大,B的体积分数增大 | |
| D. | 若反应开始时向密闭容器中充入2.4mol 的A和1.2mol 的B,达到平衡所需时间小于t |
 在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L密闭容器内,800℃时反应:2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(2)已知:K300℃>K350℃,则该反应是放热热反应.
(3)如图表示NO2的变化的曲线是b.用O2表示从0~2s内该反应的平均速率v=1.5×10-3mol•L-1•s-1.
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是c.
a.及时分离出NO2b.适当升温c.增大O2的浓度d.选择催化剂.
| 检测次数 | 溶液中检测结果 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,需要向溶液中依次滴加HNO3溶液,Ba(NO3)2溶液,AgNO3溶液.(填化学式)
