题目内容
19.某化学兴趣小组在课外活动中,对某溶液进行了多次检测,其中三次检测结果如表所示,请回答:| 检测次数 | 溶液中检测结果 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、BaCl2、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,需要向溶液中依次滴加HNO3溶液,Ba(NO3)2溶液,AgNO3溶液.(填化学式)
分析 (1)一、三次中物质在溶液中不反应,而第二次中物质可反应生成沉淀;
(2)为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,先加硝酸检验碳酸根离子,再利用硝酸钡检验硫酸根离子,最后加硝酸银检验氯离子,以此来解答.
解答 解:(1)一、三次中物质在溶液中不反应,而第二次中BaCl2分别与Na2SO4、K2CO3可反应生成硫酸钡、碳酸钡沉淀,则结果不正确,故答案为:二;
(2)在检测时,为了确定溶液中是否存在硫酸根离子、碳酸根离子和氯离子,需要向溶液中依次滴加HNO3溶液,Ba(NO3 )2溶液,AgNO3溶液,
故答案为:HNO3;Ba(NO3 )2;AgNO3.
点评 本题考查物质的鉴别和检验,为高频考点,把握常见离子之间的反应及检验方法为解答的关键,侧重分析与应用能力的考查,注意离子检验中试剂的顺序,题目难度不大.

练习册系列答案
相关题目
9.氨的合成是最重要的化工生产之一.
Ⅰ.合成氨用的氢气有多种制取的方法:
①活泼金属(如钠)直接跟水反应;
②金属(如锌)跟稀盐酸或稀硫酸反应;
③电解水制氢气
④由焦炭跟水反应制取氢气:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
⑤由天然气制取氢气:CH4+H2O(g)$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CO+3H2
(1)请你再补充一种制取氢气的方法,写出该反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(2)已知有关反应的能量变化如图,则方法⑤反应的焓变△H=(a+3b-c)kJ•mol-1.

Ⅱ.在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)$\frac{\underline{\;高温高压\;}}{催化剂}$2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如表:
(3)分析上表数据,下列关系正确的是ab(填写序号字母).
a.2c1>1.5mol/L b.2ρ1=ρ2 c.ω3=ω1
(4)在该温度下该反应的平衡常数K=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}×(3{c}_{1}-1.5)^{3}}$(用含c1的代数式表示).
(5)容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol/(L.min).
Ⅲ.用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)?CO (NH2)2(l)+H2O(g).某温度下,为进一步提高CO2的平衡转化率,下列措施中能达到目的是ab.
a.提高NH3的浓度 b.增大压强 c.及时转移生成的尿素 d.使用更高效的催化剂.
Ⅰ.合成氨用的氢气有多种制取的方法:
①活泼金属(如钠)直接跟水反应;
②金属(如锌)跟稀盐酸或稀硫酸反应;
③电解水制氢气
④由焦炭跟水反应制取氢气:C+H2O(g)$\frac{\underline{\;高温\;}}{\;}$CO+H2;
⑤由天然气制取氢气:CH4+H2O(g)$\frac{\underline{\;\;\;高温\;\;\;}}{催化剂}$CO+3H2
(1)请你再补充一种制取氢气的方法,写出该反应的化学方程式2Al+2NaOH+2H2O=2NaAlO2+3H2↑.
(2)已知有关反应的能量变化如图,则方法⑤反应的焓变△H=(a+3b-c)kJ•mol-1.

Ⅱ.在3个2L的密闭容器中,在相同的温度下、使用相同的催化剂分别进行反应:3H2(g)+N2(g)$\frac{\underline{\;高温高压\;}}{催化剂}$2NH3(g),按不同方式投入反应物,保持恒温、恒容,测得反应达到平衡时有关数据如表:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 3mol H2、2mol N2 | 6mol H2、4mol N2 | 2mol NH3 |
| 达到平衡的时间(min) | 5 | 8 | |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | |
| NH3的体积分数 | ω1 | ω3 | |
| 混合气体密度(g•L-1) | ρ1 | ρ2 |
a.2c1>1.5mol/L b.2ρ1=ρ2 c.ω3=ω1
(4)在该温度下该反应的平衡常数K=$\frac{(2-2{c}_{1})^{2}}{{c}_{1}×(3{c}_{1}-1.5)^{3}}$(用含c1的代数式表示).
(5)容器乙中反应从开始到达平衡的反应速率为v(H2)=0.3mol/(L.min).
Ⅲ.用氨气制取尿素[CO(NH2)2]的反应为:2NH3(g)+CO2(g)?CO (NH2)2(l)+H2O(g).某温度下,为进一步提高CO2的平衡转化率,下列措施中能达到目的是ab.
a.提高NH3的浓度 b.增大压强 c.及时转移生成的尿素 d.使用更高效的催化剂.
7.下列有关实验和应用的说法正确的是( )
| A. | SO2具有漂白性,可使紫色石蕊试液褪色 | |
| B. | 氧化铝、氧化镁可用作制耐火材料 | |
| C. | 可用瓷坩埚中加热熔化氢氧化钠固体 | |
| D. | 向溴水中滴入植物油,振荡后,油层显无色,说明溴不溶于油脂 |
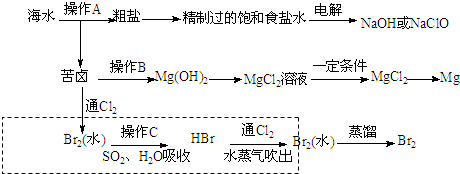
11.海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程.下列有关说法正确的是
( )

( )

| A. | 用澄清的石灰水可鉴别NaHCO3和Na2CO3 | |
| B. | 溴元素在第③、⑤中被氧化,在第④中被还原 | |
| C. | 工业上一般用金属钠与无水MgCl2反应制取Mg单质 | |
| D. | 海水中还含有碘元素,只需将海水中的碘升华就可以得到碘单质 |
9.下列各组物质,用一种试剂无法区别的是( )
| A. | 三种浓酸:HNO3、H2SO4、HCl | |
| B. | 四种黑色粉末:FeO、Fe、CuO、C | |
| C. | 四种无色溶液:NaCl、NaOH、KOH、KCl | |
| D. | 四种白色粉末:(NH4)2SO4、NH4Cl、Na2SO4、NaCl |