题目内容
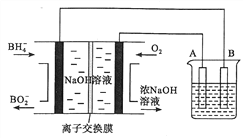
【题目】某学习小组为研究电化学原理,设计如图装置.下列叙述不正确的是( ) 
A.a和b不连接时,铁片上会有金属铜析出
B.a和b用导线连接时,铜片上发生的反应为:Cu2++2e﹣=Cu
C.a和b分别连接足够电压的直流电源正、负极时,Cu2+向铜电极移动
D.无论a和b是否用导线连接,铁片均溶解,溶液从蓝色逐渐变成浅绿色
【答案】C
【解析】解:A.a和b不连接时,发生Fe+Cu2+=Cu+Fe2+置换反应,则铁片上会有金属铜析出,故A正确;
B.a和b用导线连接时,Cu为正极,在正极上阳离子得电子,则发生Cu2++2e﹣=Cu,故B正确;
C.a和b分别连接足够电压的直流电源正、负极时,形成电解池,b与负极相连为阴极,阳离子向阴极移动,所以Cu2+向Fe电极移动,故C错误;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+,则铁片均溶解,溶液从蓝色逐渐变成浅绿色,故D正确;
故选C.
A.a和b不连接时,发生置换反应;
B.a和b用导线连接时,Cu为正极,在正极上阳离子得电子;
C.a和b分别连接足够电压的直流电源正、负极时,形成电解池,b为阴极,阳离子向阴极移动;
D.无论a和b是否用导线连接,均发生Fe+Cu2+=Cu+Fe2+.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案
相关题目