题目内容
9.下列金属中,按照金属性从弱到强的顺序排列的是( )| A. | 铝、镁、钠、钾 | B. | 镁、铝、钾、钠 | C. | 钙、钾、铷、钠 | D. | 钙、钾、钠、锂 |
分析 同周期主族元素,自左而右随原子序数增大金属性减弱;同主族元素,自上而下随电子层增大金属性增强.据此判断.
解答 解:A、铝、镁、钠处于同周期,原子序数依次较小,所以金属性铝<镁<钠;钠、钾处于同主族,钾电子层多,失电子能力增强,金属性钠<钾,所以金属性铝<镁<钠<钾,故A正确;
B、由A中分析可知金属性铝<镁<钠<钾,故B错误;
C、钙、钾处于同周期,原子序数依次较小,所以金属性钙<钾;钠、钾、铷处于同主族,电子层依次增多,失电子能力增强,所以金属性钠<钾<铷,所以金属性钠<钙<钾<铷,故C错误;
D、钙、钾处于同周期,原子序数依次较小,所以金属性钙<钾;钾、钠、锂处于同主族,电子层依次减少,失电子能力减弱,所以金属性钾>钠>锂,由金属活动顺序表可知金属性钙>钠,所以金属性钾>钙>钠>锂,故D错误.
故选:A.
点评 本题考查金属性强弱的判断,难度不大,注意元素周期律的运用.

练习册系列答案
 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
20.某同学按图所示的装置进行电解实验.下列说法正确的是( )
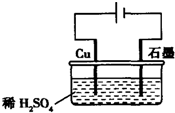

| A. | 电解过程中,铜电极上有H2产生 | |
| B. | 电解初期,主要反应方程式为:Cu+H2SO4$\frac{\underline{\;电解\;}}{\;}$CuSO4+H2↑ | |
| C. | 电解一定时间后,石墨电极上有铜析出 | |
| D. | 整个电解过程中,H+的浓度不断增大 |
17.下列叙述都涉及化学相关知识,其中正确的是( )
| A. | 在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液 | |
| B. | 10 g46%的乙醇水溶液中所含氢原子数目为1.2NA | |
| C. | 200 ml1mol/LFe2(SO4 )3溶液中,Fe3+和SO42-离子数的总和是NA | |
| D. | 可用电解氯化镁溶液的方法制取金属镁 |
4.在NH4Cl饱和溶液中分别加入①Mg;②NH4Cl(固);③NH4HCO3;④H2O;⑤氯水;⑥Cu.能使该溶液的pH值增大的是( )
| A. | ②③ | B. | ①②⑤ | C. | ②③⑥ | D. | ①③④ |
1. 今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )
今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )
 今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )
今年两会的一个主题是环境保护,治理雾霾天气是我们目前最主要的一个任务.如图是北京统计的雾霾天气的来源和成分分析:下列对于治理雾霾天气措施描述不正确的是( )| A. | 充分的洗涤燃煤,除去燃煤表面的灰尘 | |
| B. | 加快我国由“燃煤”时代进入到“油气”时代的步伐 | |
| C. | 采用催化转换技术将汽车尾气中的NO2和CO转化为无毒气体 | |
| D. | 处理NO2的一种方法是利用甲烷催化还原NO2,若CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g);△H=-512kJ•mol-1,则1g甲烷处理NO2需要放出16kJ的热量 |
18.下列各组中的反应,属于同一反应类型的是( )
| A. | 由溴丙烷水解制丙醇;由丙烯与水反应制丙醇 | |
| B. | 由甲苯硝化制对硝基甲苯;由甲苯氧化制苯甲酸 | |
| C. | 由氯代环己烷消去制环己烯;由乙醇制乙烯 | |
| D. | 由乙酸和乙醇制乙酸乙酯;由苯甲酸乙酯水解制苯甲酸和乙醇 |
19.A、B两种原子,A原子M层比B原子M层少3个电子,B原子L层电子数恰好是A原子L层的两倍,则A元素是( )
| A. | O | B. | Si | C. | C | D. | Mg |

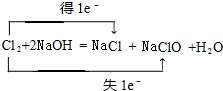 ;
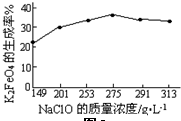
;
 所示.
所示. 出发来合成M,其合成路线如下:
出发来合成M,其合成路线如下:
 .
. .
. +2Cu(OH)2$\stackrel{△}{→}$
+2Cu(OH)2$\stackrel{△}{→}$ +Cu2O↓+2H2O.
+Cu2O↓+2H2O.