题目内容
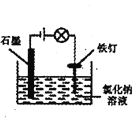
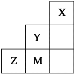
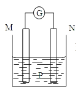
【题目】在如图所示装置中,观察到电流计指针偏转,M棒变细,N棒变粗,其中P为电解质溶液。由此判断M、N、P所代表的物质不可能是( )
M | N | P | |
A | Zn | Cu | 稀硫酸 |
B | Fe | Cu | 硫酸铜溶液 |
C | Zn | Ag | 硝酸银溶液 |
D | Zn | Fe | 硝酸铜溶液 |
A.AB.BC.CD.D
【答案】A
【解析】
由装置图可知,该装置为原电池,M棒变细,N棒变粗,说明M为原电池的负极,N为原电池的正极,据此分析判断。
A. M为Zn,N为Cu,电解质溶液为稀硫酸时,Zn为负极,逐渐变细,Cu为正极,由于电解质溶液为稀硫酸,所以在Cu棒表面会产生大量的气泡,A项错误,符合题意;
B. M为Fe,N为Cu,电解质溶液为硫酸铜时,Fe为负极,逐渐变细,Cu为正极,由于电解质溶液为硫酸铜,所以Cu2+得到电子生成Cu,附着在铜棒表面,使铜棒变粗,B项正确,不符合题意;
C. M为Zn,N为Ag,电解质溶液为硝酸银时,Zn为负极,逐渐变细,Ag为正极,由于电解质溶液为硝酸银,所以Ag得到电子生成Ag,附着在银棒表面,使银棒变粗,C项正确,不符合题意;
D. M为Zn,N为Fe,电解质溶液为硝酸铜时,Zn为负极,逐渐变细,Fe为正极,由于电解质溶液为硝酸铜,所以在Cu2+得到电子生成Cu,附着在铁棒表面,使铁棒变粗,D项正确,不符合题意;
答案选A。

 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案【题目】甲醇是重要的化工原料。在催化剂的作用下,利用合成气(主要成分为CO、CO2和H2)合成甲醇的主要化学反应如下:
Ⅰ.CO+2H2![]() CH3OH
CH3OH
Ⅱ.CO2+3H2![]() CH3OH+H2O
CH3OH+H2O
Ⅲ.CO2+H2![]() CO+H2O
CO+H2O
请回答下列问题:
(1)已知三种物质的标准燃烧热如下表:
物质 | CO(g) | H2(g) | CH3OH(l) |
燃烧热(kJ·mol1) | 283.0 | 285.8 | 726.5 |
①书写25℃、101kPa条件时CO燃烧热的热化学方程式____________。
②计算25℃、101kPa条件时反应Ⅰ的ΔH=_____kJ·mol1 。
(2)甲醇燃料电池(Direct Methanol Fuel Cell)属于质子交换膜燃料电池,其工作原理如图所示:

①c处产生的气体是_______________;
②负极的电极反应式是_______________。
(3)下图是甲醇燃料电池工作示意图,其中A,B,D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A,B两极上产生的气体体积相同。
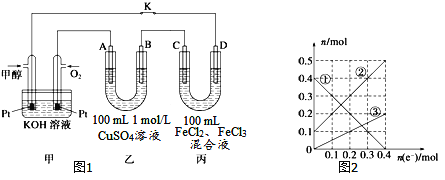
①乙中B极的电极反应式_______。
②乙中A极析出的气体在标况下的体积________。
③丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如图,则②线表示的是____的变化,反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要____mL 5mol/LNaOH溶液。
(4)蓄电池是一种反复充电、放电的装置。有一种蓄电池在充电和放电时发生的反应如下:NiO2+Fe+2H2O![]() Fe(OH)2+Ni(OH)2。
Fe(OH)2+Ni(OH)2。
①此蓄电池在充电时,电池负极应与外加电源的________极连接。
②放电时正极的电极反应式为_____________________。
(5)按如图所示装置进行下列不同的操作
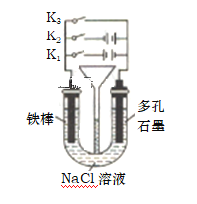
①将K1 、K2、 K3分别只关闭一个,则铁的腐蚀的速度最快的是只闭合_____(填“K1”或 “K2”或“K3”,下同),为减缓铁的腐蚀, 只闭合_____,该防护法称为______________。
②只闭合K3,当铁棒质量减少5.6g时,石墨电极消耗的气体体积为__________L(标准状况)。
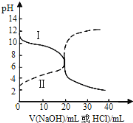
【题目】在100℃时,将0.1mol的四氧化二氮气体充入1 L抽空的密闭容器中,发生反应,隔一定时间对该容器内的物质进行分析,得到如下数据:
浓度 时间(S) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4)/mol·L—1 | 0.1 | c1 | 0.05 | c3 | a | b |
c(NO2)/mol·L—1 | 0 | 0.06 | c2 | 0.12 | 0.12 | 0.12 |
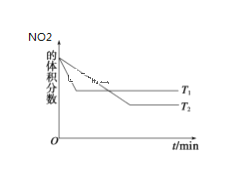
(1)该反应的化学方程式为______________________,表中c2_____c3_____a______b(选填“>”、“<”、“==”)。
(2)20 s时四氧化二氮的浓度c1=____________mol·l—1依据图象可以判断该反应的 ΔH___0(填“>”或“<”)