题目内容
18.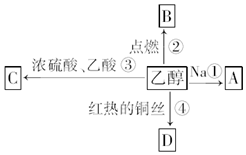 乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是有机物.
乙醇是生活中常见的有机物,能进行如图所示的多种反应,A、B、C、D都是有机物.(1)写出下列反应的化学方程式
反应①:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
反应②:C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O
反应③:CH3CH2OH+CH3COOH
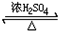 CH3COOCH2CH3+H2O
CH3COOCH2CH3+H2O反应④:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O
(2)比较反应①与钠和水反应的现象有什么相同和不同
相同点:都有无色气泡产生,都有热量放出
不同点:乙醇与钠反应时,钠沉在液面下,反应也更平稳.
分析 乙醇结构简式为CH3CH2OH,含有羟基,与钠发生反应生成A为CH3CH2ONa,乙醇醇羟基能与乙酸发生酯化反应生成C为CH3COOCH2CH3,乙醇含有碳氢氧,能和氧气发生燃烧反应生成二氧化碳和水,乙醇含有醇羟基能和氧气在铜作催化剂的作用下发生催化氧化反应,
(1)①醇羟基中的氢原子和钠发生置换反应生成醇钠和氢气;
②碳氢氧和氧气反应生成二氧化碳和水;
③反应本质为:酸脱羟基醇脱氢;
④乙醇羟基上的氢原子和与羟基相连的碳上分别脱掉一个氢与氧原子生成水;
(2)乙醇与钠反应生成乙醇钠与氢气,钠的密度比乙醇大,钠沉在液面下,乙醇中羟基氢不如水中的活泼,不如钠与水的反应剧烈,反应也更平稳;
解答 解:乙醇结构简式为CH3CH2OH,含有羟基,与钠发生反应生成A为CH3CH2ONa,乙醇醇羟基能与乙酸发生酯化反应生成C为CH3COOCH2CH3,乙醇含有碳氢氧,能和氧气发生燃烧反应生成二氧化碳和水,乙醇含有醇羟基能和氧气在铜作催化剂的作用下发生催化氧化反应,
(1)①钠是活泼金属,乙醇与钠发生置换反应,生成醇乙醇钠与氢气,反应方程式为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,
故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
②乙醇能和氧气反应生成水和二氧化碳,反应的化学方程式为:C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O,
故答案为:C2H5OH+3O2$\stackrel{点燃}{→}$2CO2+3H2O;
③乙醇与乙酸在浓硫酸、加热条件下发生酯化反应生成乙酸乙酯与水,反应方程式为:CH3CH2OH+CH3COOH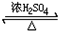 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:CH3CH2OH+CH3COOH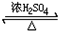 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
④乙醇在铜作催化剂、加热条件下,乙醇羟基上的氢原子和与羟基相连的碳上分别脱掉一个氢与氧原子生成水,反应方程式为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O,
故答案为:2CH3CH2OH+O2$→_{△}^{Cu}$2CH3CHO+2H2O;
(2)Na与水、乙醇反应,均生成氢气,放出热量,但Na的密度比乙醇大,Na沉在乙醇液面下,乙醇中羟基不如水中活泼,反应较水更平稳,故
相同点:都有无色气泡产生,都有热量放出;
不同点:乙醇与钠反应时,钠沉在液面下,反应也更平稳,
故答案为:都有无色气泡产生,都有热量放出;乙醇与钠反应时,钠沉在液面下,反应也更平稳.
点评 本题考查有机的推断,涉及醇、羧酸的性质与转化等,是对常见有机物知识的运用,注有利于基础知识的巩固,掌握乙醇醇羟基官能团的性质是解答该题的关键,题目难度不大.

| A. | 上述气态化合物分子中所有原子最外层电子数均为8 | |
| B. | X、Y、Z都可与W形成既有极性共价键又有非极性共价键的化合物 | |
| C. | 化合物W4XY2Z可能是离子化合物,也可能是共价化合物 | |
| D. | 沸点:W2Z>YW3>XW4 |
| A. | HCO3-+H2O?H3O++CO32- | B. | HS-+H2O?H2S+OH- | ||
| C. | H2PO4-+H2O?HPO42-+H3O+ | D. | HCO3-+OH-?H2O+CO32- |
①CH2=CHCH3②
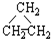 ③CH3CH2CH3 ④HC≡CCH3 ⑤
③CH3CH2CH3 ④HC≡CCH3 ⑤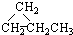 ⑥CH3CH=CHCH3.
⑥CH3CH=CHCH3.| A. | ①和② | B. | ①和③ | C. | ①和④ | D. | ④和⑥ |
| A. | 9.6g | B. | 6.4g | C. | 3.2g | D. | 1.6g |
| A. | 放热183 kJ | B. | 放热91.5 kJ | C. | 吸热183 kJ | D. | 吸热91.5 kJ |
| A. | -770 kJ/mol | B. | -l220 kJ/mol | C. | -1500kJ/mol | D. | -2740kJ/mol |
| A. | 第n周期的最后一种金属元素处在第n-1族(1<n<7,n为正整数) | |
| B. | m=1和m=7(m为最外层电子数)的元素单质能形成的化合物都是离子化合物 | |
| C. | m-n=5(m为最外层电子数,n为电子层数)的主族元素存在最强的对应含氧酸 | |
| D. | 第n周期有n种主族金属元素(1<n<7,n为正整数) |
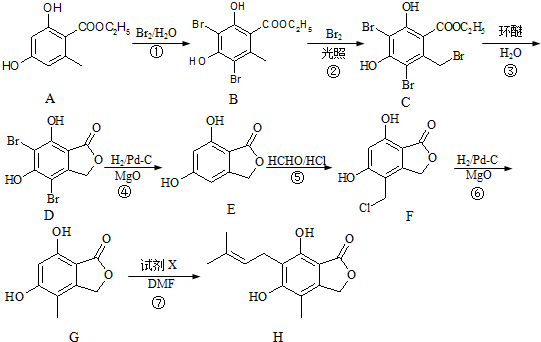
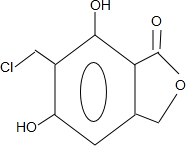 (任写一种).
(任写一种).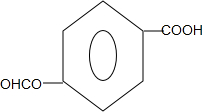 .
.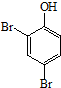 、HCHO为原料制备
、HCHO为原料制备 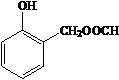 合成路线流程图(无机试剂任用).合成路线流程图示例如下:
合成路线流程图(无机试剂任用).合成路线流程图示例如下: