题目内容
【题目】某化学兴趣小组对Fe3O4产生了兴趣,从参考资料中找到了氧化沉淀法生产复印用高档Fe3O4粉的工艺流程简图:
 【查阅资料】
【查阅资料】
资料一:硫酸亚铁在不同温度下的溶解度如表所示:
温度/℃ | 0 | 10 | 30 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.3 | 33.0 | 30.5 | 27.0 |
资料二:Fe(OH)2受氧气氧化反应原理为:4Fe(OH)2 +2H2O+O2=4Fe(OH)3
资料三:获得Fe3O4的反应原理为:Fe(OH)2 + 2Fe(OH)3 ![]() Fe3O4+4H2O
Fe3O4+4H2O
Ⅰ【问题讨论】
(1)溶解时,用50℃至80℃的热水目的是__________________________________________。
(2)副产品P是___________________________。
(3)为了得到纯净的产品,过滤、洗涤后进行的具体操作过程为______________________________、干燥
Ⅱ【组成确定】
资料显示:①铁的氢氧化物在受热时分解生成铁的氧化物(化合物不变);
②Fe2O3和CO反应是随温度升高而逐步进行的,先生成Fe3O4,再生成FeO(黑色),最后生成Fe。
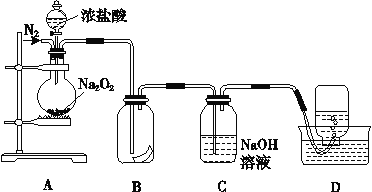
为确定用以上方法制得的四氧化三铁的纯度,同学们称取了23.28g该Fe3O4样品设计下列实验进行探究。

(1)该组同学欲通过称量B装置反应前后的质量变化来计算确认该Fe3O4样品中的杂质。B中的最佳试剂是_______________________(填序号)。
A.澄清石灰水 B.氢氧化钠浓溶液 C.稀盐酸 D.水
(2)上述实验过程中,CO气体除作为反应物外,能起到的作用还有:
①实验开始时,排尽装置中的空气,防止加热时发生爆炸;
②停止加热后,继续通CO气体,防止生成物被氧化,以及B中的溶液倒吸入A中;且可以_____________________________,以提高实验的精确度。
(3)利用仪器测定并绘制出反应过程中

①该Fe3O4样品中含有的杂质成分______________________(填化学式)
②计算样品中Fe3O4的质量分数(写出必要的计算过程)。 _____________
【答案】 该温度时硫酸亚铁的溶解度较大 Na2SO4 取最后一次洗涤的滤液于试管中,加入(盐酸酸化的)BaCl2溶液,若无白色沉淀,说明已经洗涤干净 B 将产生的CO2全部赶入装置B中 Fe2O3 设Fe2O3和Fe3O4的物质的量分别为x、y,根据铁原子守恒有2x+3y=16.80/56mol =0.3mol ,根据质量有:160x+232y=23.28,所以解得y=0.09mol,故样品中Fe3O4的质量分数=0.09×232g÷23.28g×100%=89.69%。
【解析】Ⅰ(1)根据FeSO4的溶解度表可知,50℃至80℃时FeSO4的溶解度较大,其他温度下溶解度较小,不利于溶解,故答案为:该温度时硫酸亚铁的溶解度较大。
(2)FeSO4与NaOH反应除了生成Fe(OH )2,还生成Na2SO4,故副产物P为Na2SO4。
(3)沉淀的成分为Fe(OH)2和Fe(OH)3,其中含有杂质Na2SO4,要得到纯净的产品,必须将沉淀洗涤干净,因此过滤、洗涤后进行的操作过程为:取最后一次洗涤的滤液于试管中,加入盐酸酸化的BaCl2溶液,若无白色沉淀,说明已经洗涤干净。
Ⅱ(1)CO和Fe3O4反应生成CO2气体,吸收CO2气体的最好的试剂为NaOH溶液,故B中的最佳试剂为NaOH,答案为B。
(2)CO还可以将产生的CO2气体全部赶入装置B中,提高实验的准确率,故答案为:将产生的CO2全部赶入装置B中。
(3)①若样品中只有Fe3O4,加热过程中固体质量下降应只有两段,而现在样品的质量下降有三段,故样品中除了Fe3O4外还有其他成分,沉淀M为Fe(OH)2和 Fe(OH)3的混合物,加热时除生成Fe3O4外,Fe(OH)3加热分解能生成Fe2O3,故Fe3O4样品中含有的杂质成分为Fe2O3。 ②设Fe2O3和Fe3O4的物质的量分别为x、y,根据铁原子守恒有2x+3y=(16.80/56)mol =0.3mol ,根据质量有:160x+232y=23.28,所以解得y=0.09mol,故样品中Fe3O4的质量分数=0.09×232g÷23.28g×100%=89.69%。

【题目】实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] 有关物质性质如下:
甘氨酸(NH2CH2COOH) | 柠檬酸 | 甘氨酸亚铁 |
易溶于水,微溶于乙醇,两性化合物 | 易溶于水和乙醇,有强酸性和还原性 | 易溶于水,难溶于乙醇 |
实验过程:
Ⅰ.配制含0.10mol FeSO4的绿矾溶液。
Ⅱ.制备FeCO3:向配制好的绿矾溶液中,缓慢加入200mL 1.1mol·L-1NH4HCO3溶液,边加边搅拌,反应结束后过滤并洗涤沉淀。
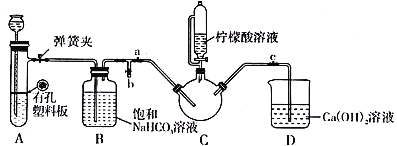
Ⅲ.制备(NH2CH2COO)2Fe:实验装置如下图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。
回答下列问题:
(1)实验I中:实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为_______(写化学式)。再滴加少量稀硫酸的作用是__________________________。
(2)实验II中:生成沉淀的离子方程式为__________________________。
(3)实验Ⅲ中:①C中盛柠檬酸溶液的仪器名称为___________________。
②装置A中所盛放的药品是___________________。(填序号)
A.Na2CO3和稀H2SO4 B.CaCO3和稀H2SO4 C.CaCO3和稀盐酸
③确认C中空气排尽的实验现象是____________________。
④加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是________________。
⑤洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是___________________。(填序号)
A.热水 B.乙醇溶液 C.柠檬酸溶液
⑥若产品的质量为17.34g,则产率为________%。